Primer estudio prospectivo observacional del mundo real que evalúa el teplizumab en diabetes tipo 1 en estadio 2, y aporta datos completos sobre su administración y los efectos clínicos
Lugones Editorial©
En noviembre de 2022, la FDA aprobó el teplizumab como la primera inmunoterapia modificadora de la enfermedad para la diabetes tipo 1 (DM1). Se trata de un anticuerpo monoclonal humanizado dirigido contra CD3, un componente clave del complejo del receptor de células T (TCR) involucrado en la activación y señalización de las células T.
La unión del teplizumab a CD3 produce un agotamiento parcial de las células T CD8+ y limita la expansión de linfocitos autorreactivos. Esta terapia está indicada para retrasar la progresión a DM1 en estadio 3 en niños y adultos de 8 años o más con DM1 en estadio 2, según lo definido por los criterios de la ADA.
Un ensayo clínico previo demostró que la administración de teplizumab durante 14 días consecutivos en personas con DM1 en etapa 2 retrasó significativamente la progresión a estadio 3, con una mediana de retraso de aproximadamente 24 meses, que se extensión hasta más de 32 meses en análisis de seguimiento prolongado. Sin embargo, la evidencia disponible proviene principalmente de ensayos clínicos controlados.
Dado que los ensayos clínicos se desarrollan en poblaciones seleccionadas y en condiciones altamente controladas, existe una necesidad crítica de generar datos del mundo real. Evaluar el uso clínico del teplizumab en la práctica habitual resulta fundamental para determinar si sus beneficios se reproducen en poblaciones más heterogéneas y en entornos asistenciales de rutina.

El objetivo de este estudio fue aportar datos completos del mundo real sobre la administración y los efectos clínicos del tratamiento con teplizumab
Materiales y métodos
- Estudio de cohorte observacional prospectivo de mundo real realizado en el Barbara Davis Center for Diabetes. Se incluyeron niños y adultos con DM1en estadio 2 tratados con teplizumab entre abril de 2023 y febrero de 2025.
- Para comparación contextual, se identificó un grupo no tratado de 10 individuos con DM1 en estadio 2, previamente seguidos en el mismo centro bajo protocolos clínicos similares, que no recibieron teplizumab por cuestiones de disponibilidad o elegibilidad temporal.
- La DM1 en estadio 2 se definió por la presencia de disglucemia y autoanticuerpos de islotes (IAA, GADA, IA-2A y/o ZnT8A). La disglucemia se evaluó mediante HbA1c y/o prueba de tolerancia oral a la glucosa (oral glucose tolerance test, OGTT).
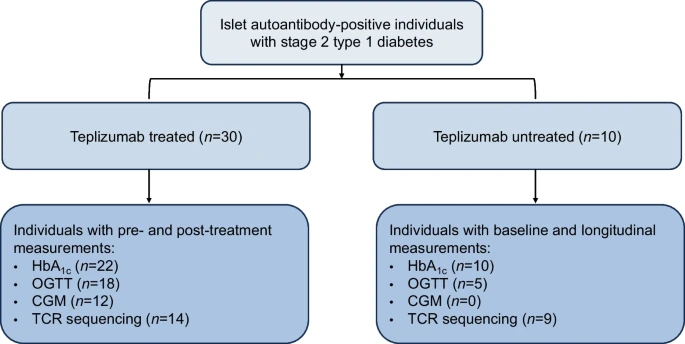
Diagrama de flujo de participantes y recopilación de datos
- Se recopilaron datos demográficos y clínicos al inicio y durante el seguimiento. Las evaluaciones incluyeron HbA1c, OGTT y péptido C, con visitas de seguimiento recomendadas a los 3 y 6 meses y luego cada 6 meses, aunque los intervalos reales variaron según la práctica clínica habitual.
- Se analizaron datos de MCG antes y después del tratamiento con teplizumab. Los datos se agruparon en intervalos trimestrales y se evaluaron métricas glucémicas clave, con especial énfasis en el tiempo por encima de 7,8 mmol/l, un umbral asociado a mayor riesgo de progresión a DM1 en estadio 3.
Resultados
Características basales y curso del tratamiento con teplizumab
Se incluyeron 30 personas con DM1 en estadio 2 tratadas con teplizumab en un centro especializado de referencia, junto con un grupo comparador de 10 individuos no tratados.
La cohorte tratada fue mayoritariamente femenina, con una mediana de edad de 18,1 años, y mostró una alta proporción de pacientes blancos y con seguro privado. Las características demográficas, inmunológicas y genéticas basales fueron similares entre los grupos tratados y no tratados, incluyendo edad, sexo, prevalencia de autoanticuerpos de islotes y perfiles HLA-DR.
Sin embargo, el grupo tratado con teplizumab presentaba una disglucemia más avanzada al inicio, con valores significativamente más elevados de HbA1c y de glucosa a las 2 horas del OGTT en comparación con el grupo no tratado. Asimismo, en comparación con el ensayo TN10, los pacientes tratados en este estudio del mundo real mostraron niveles basales de glucosa OGTT más altos, lo que sugiere una población clínicamente más comprometida.
Todos los participantes completaron los 14 días consecutivos de infusión intravenosa de teplizumab. El perfil de seguridad fue consistente con estudios previos, con efectos adversos frecuentes pero previsibles, principalmente linfopenia transitoria, náuseas, leucopenia, erupción cutánea y elevación leve de enzimas hepáticas. No se registraron eventos adversos graves.
| Personas tratadas con teplizumab con DM1 en estadio 2 (n=30) | Personas no tratadas con DM1 en estadio 2 (n=10) | Estudio TN10: grupo tratado con teplizumab (n=44) | Estudio TN10: grupo placebo (n=32) | |
| Edad en la primera visita, años (IQR) | 18 (13-30) | 18 (13-25) | 14 (12–22) | 13 (11-16) |
| Sexo, femenino, n (%) | 16 (53) | 4 (40) | 19 (43) | 15 (47) |
| Raza, Blanco, n (%) | 28 (93) | 10 (100) | 44 (100) | 30 (94) |
| HbA1c, mmol/mol (IQR) | 39 (36-43)* | 36 (33-37)* | 33 (30-36) | 34 (32-36) |
| HbA1c, % (IQR) | 5,7 (5,4–6,1)* | 5.4 (5.2–5.5)* | 5.2 (4,9–5,4) | 5.3 (5,1−5,4) |
| OGTT 2 h glucosa, mmol/l | 10,7 ± 2,1 * | 8,6 ± 2,2* | 8,5 ± 1,4 | 8,3 ± 1,6 |
| Autoanticuerpos de isleta, n (%) | ||||
| IAA | 14 (47) | 6 (60) | 20 (45) | 11 (34) |
| GADA | 29 (97) | 10 (100) | 40 (91) | 28 (88) |
| IA-2A | 23 (77) | 7 (70) | 27 (61) | 24 (75) |
| ZnT8A | 21 (70) | 7 (70) | 32 (73) | 24 (75) |
| Número de autoanticuerpos de islotes positivos, n (%) | ||||
| Uno | 1 (3) | 2 (20) | 1 (2) | 0 (0) |
| Dos | 10 (33) | 1 (10) | 11 (25) | 7 (22) |
| Tres | 10 (33) | 2 (20) | 12 (27) | 5 (16) |
| Cuatro | 9 (30) | 5 (50) | 20 (46) | 20 (63) |
| Genotipos HLA-DR, n (%) | ||||
| DR3 y DR4 | 5 (17) | 3 (30) | 11 (25) | 7 (22) |
| Solo DR4 | 19 (63) | 6 (60) | 17 (39) | 14 (44) |
| Solo DR3 | 3 (10) | 1 (10) | 10 (23) | 8 (25) |
| Ni DR3 ni DR4 | 2 (7) | 0 (0) | 5 (11) | 3 (9) |
Características clínicas, metabólicas e inmunológicas de los participantes del estudio actual y del estudio TN10 al inicio
Progresión a diabetes tipo 1 en estadio 3
Durante un seguimiento medio cercano a los 10 meses, solo el 13% de los individuos tratados con teplizumab progresaron a DM1 en estadio 3, frente al 30% en el grupo no tratado, en un período de observación comparable. Ningún participante tratado desarrolló cetoacidosis diabética, y todos los que progresaron mantuvieron requerimientos bajos de insulina, lo que sugiere una preservación parcial de la función beta.
Mejora y estabilización de las medidas glucémicas
En los individuos tratados con teplizumab que contaban con OGTT emparejados antes y después del tratamiento, se observó una reducción significativa de la glucosa a las 2 horas del OGTT a los 2–6 meses, con mantenimiento de valores similares a los basales a más largo plazo. En contraste, el grupo no tratado no mostró cambios significativos en las mediciones de OGTT durante el seguimiento.
La categorización de los OGTT evidenció una mejora significativa del estado glucémico en el grupo tratado, con transición desde hiperglucemia o disglucemia hacia euglucemia en un número relevante de pacientes. La secreción de insulina, evaluada mediante el AUC del péptido C, se mantuvo estable tras el tratamiento, sin evidencia de deterioro funcional.
La HbA1c disminuyó de forma significativa tras el tratamiento con teplizumab y esta reducción se mantuvo durante el seguimiento, mientras que en el grupo no tratado se observó una tendencia al empeoramiento del control glucémico. Asimismo, el número de individuos con HbA1c en rango de disglucemia se mantuvo estable en el grupo tratado, pero aumentó en el grupo no tratado.
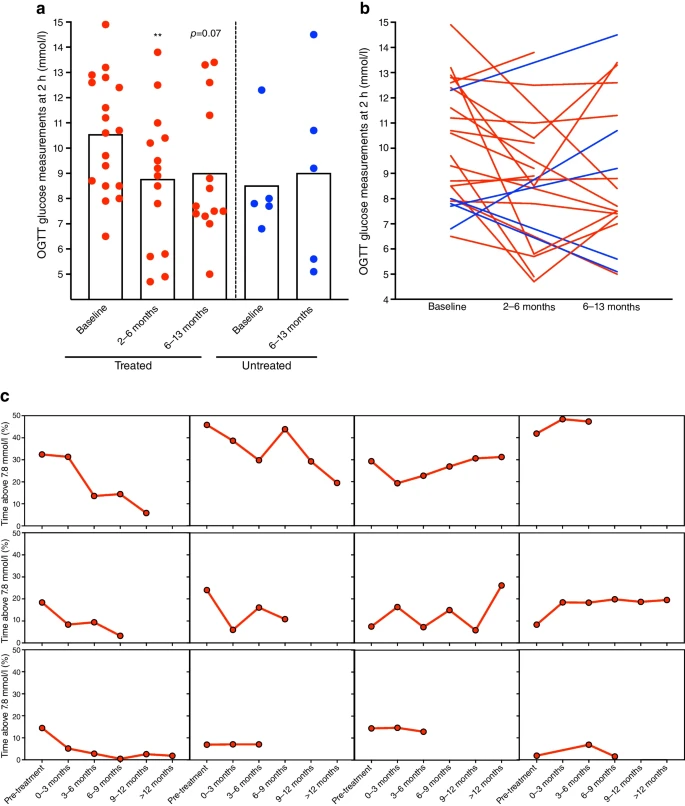
Resultados de OGTT y del MCG al inicio y después del tratamiento
Datos del monitoreo continuo de glucosa
En un subgrupo con datos completos de MCG, la mayoría de los individuos tratados mostró estabilidad o reducción del tiempo con glucosa por encima de 7,8 mmol/l tras el tratamiento. Entre aquellos con mayor carga de disglucemia basal, una proporción significativa logró reducir el tiempo en rango hiperglucémico por debajo del umbral de riesgo.
Considerando conjuntamente OGTT, HbA1c y CGM, el tratamiento con teplizumab se asoció con una estabilización o mejora global del perfil glucémico en esta cohorte del mundo real.
Cambios inmunológicos inducidos por teplizumab
El análisis inmunológico mediante secuenciación profunda del repertorio TCRβ mostró que el número total de clonotipos TCR se mantuvo estable tras el tratamiento. Sin embargo, se observó una reducción selectiva de clonotipos específicos de antígenos de islotes, particularmente aquellos dirigidos contra preproinsulina (PPI), mientras que los clonotipos específicos de antígenos virales, como EBV, no se modificaron.
Este efecto fue específico del tratamiento, ya que no se observaron cambios similares en el grupo no tratado. La reducción de los clonotipos autorreactivos fue más pronunciada en determinados individuos, lo que sugiere heterogeneidad en la respuesta inmunológica al teplizumab.
Correlación entre respuesta inmune y función beta
La disminución de los clonotipos TCR específicos de PPI se correlacionó de forma significativa con valores más altos de AUC del péptido C tras el tratamiento, lo que indica una asociación entre la modulación inmunológica inducida por teplizumab y la preservación de la función de las células beta.
Esta correlación no se observó para los clonotipos específicos de antígenos virales, reforzando la especificidad del efecto inmunomodulador del fármaco.
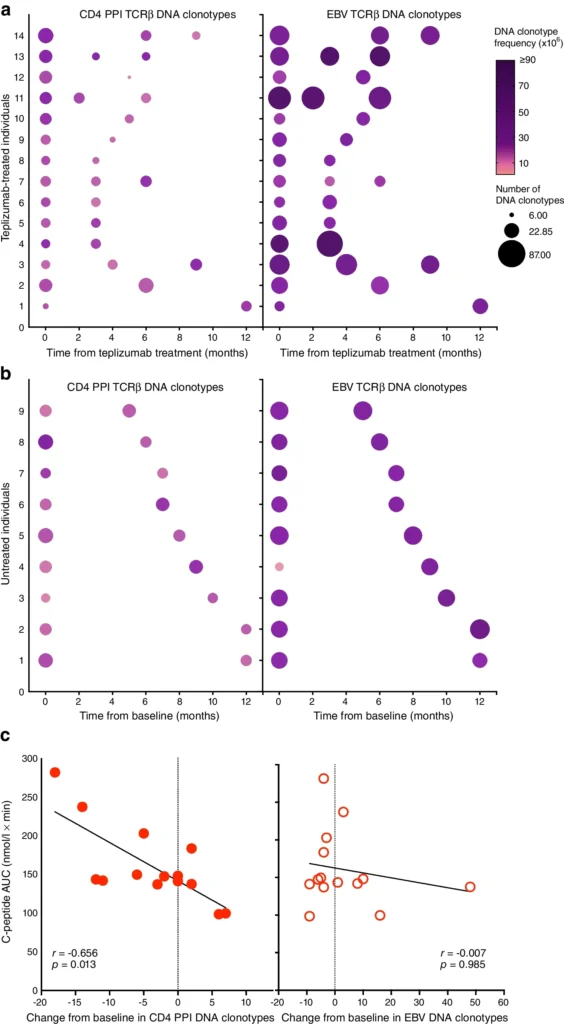
Después del tratamiento con teplizumab, se reducen los clonotipos de TCRβ específicos de PPI, lo que se correlaciona con la función de las células beta
Discusión
Este estudio aporta la primera evidencia sistemática del mundo real que demuestra que el teplizumab puede administrarse de forma segura y efectiva en la práctica clínica habitual en personas con DM1 en estadio 2.
Los autores documentan beneficios metabólicos tempranos, con mejoría de la tolerancia a la glucosa y estabilidad de la HbA1c y del péptido C durante el primer año posterior al tratamiento, reforzando el potencial del teplizumab como terapia modificadora de la enfermedad fuera del contexto estrictamente controlado de los ensayos clínicos.
- Concordancia con ensayos clínicos previos y validación en la práctica clínica
Los hallazgos observados en esta cohorte del mundo real son consistentes con los resultados del ensayo TN10, en el que el tratamiento con teplizumab se asoció con una mayor estabilidad de las categorías del OGTT y una menor progresión hacia perfiles hiperglucémicos en comparación con placebo. En este estudio, las categorías del OGTT mejoraron o se mantuvieron estables dentro del primer año posterior al tratamiento, lo que refuerza la validez externa de los datos de los ensayos clínicos y confirma el beneficio del teplizumab en la DM1 en estadios tempranos.
- Incorporación de métricas del MCG como aporte innovador
Un aporte novedoso de este trabajo es la evaluación, por primera vez, de cambios en métricas de del MCG tras el tratamiento con teplizumab. Si bien el OGTT continúa siendo la herramienta con mayor capacidad predictiva para la progresión a DM1 en estadio 3, el MCG emerge como una alternativa práctica y menos invasiva para el seguimiento en el mundo real. En este estudio, el 67% de los individuos mostró mejoría en el porcentaje de tiempo por encima de 7,8 mmol/l tras el tratamiento, una métrica que ha demostrado relevancia en etapas tempranas de la enfermedad. No obstante, los autores señalan la necesidad de un seguimiento más prolongado para definir con mayor precisión el valor pronóstico de estas métricas en relación con la respuesta al teplizumab.
La HbA1c disminuyó de forma significativa luego del tratamiento con teplizumab y esta reducción se mantuvo durante el seguimiento
- Modulación inmunológica selectiva: impacto sobre células T autorreactivas
Desde el punto de vista inmunológico, el estudio ofrece información novedosa sobre la respuesta específica a nivel del repertorio de receptores de células T (TCR). La secuenciación profunda mostró estabilidad global del repertorio de TCR, pero una reducción selectiva de clonotipos CD4 específicos de proinsulina (PPI) dentro del primer año tras el tratamiento con teplizumab. Este efecto no se observó en individuos no tratados y fue específico de los clonotipos autorreactivos, ya que los clonotipos específicos para el virus de Epstein-Barr (EBV) permanecieron estables en ambos grupos.
- Relación entre respuesta inmune y preservación de la función beta
Un hallazgo particularmente relevante es la correlación entre la reducción de clonotipos CD4 específicos de PPI y los valores del AUC del péptido C tras el tratamiento, lo que vincula directamente la modulación inmunológica con la preservación de la función de las células beta. Esta asociación no se observó con los clonotipos específicos de EBV, lo que refuerza la especificidad del efecto del teplizumab sobre la autoinmunidad relacionada con la DM1. Estos resultados amplían observaciones previas de otros inmunomoduladores, como el alefacept, y destacan la importancia de monitorizar respuestas inmunes específicas de células T CD4 frente a antígenos de islotes como potenciales biomarcadores de respuesta terapéutica.
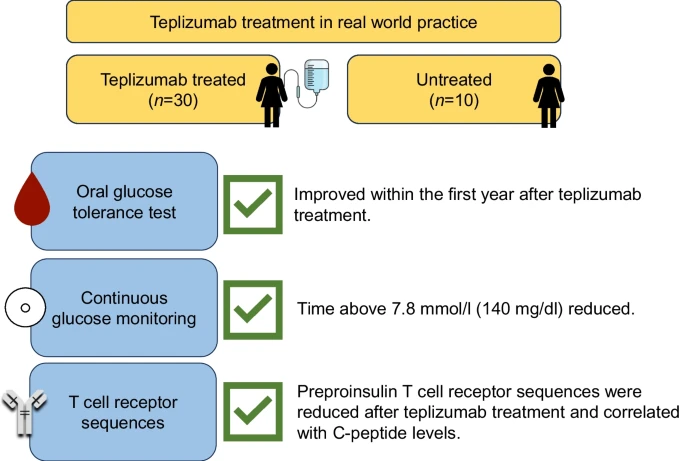
El estudio sugiere que el teplizumab se puede administrar de forma segura y eficaz en la práctica clínica
Conclusiones
Este estudio del mundo real demuestra que el tratamiento con teplizumab en personas con DM1 en estadio 2 se asocia con una mejoría temprana de los parámetros glucémicos y con una estabilidad metabólica durante el primer año posterior a su administración. Los datos metabólicos, evaluados mediante OGTT, HbA1c y CGM, respaldan los beneficios observados previamente en ensayos clínicos.
Desde el punto de vista inmunológico, el trabajo aporta evidencia innovadora de una reducción selectiva de clonotipos TCR CD4 específicos de proinsulina, que se correlaciona con la preservación del péptido C, estableciendo un vínculo directo entre modulación inmune y función beta pancreática.
En conjunto, estos hallazgos refuerzan el rol del teplizumab como una terapia modificadora de la enfermedad en etapas tempranas de la DM1 y subrayan la necesidad de estudios prospectivos más amplios y con seguimiento prolongado para confirmar la durabilidad de sus efectos metabólicos e inmunológicos en el mundo real.
Se refuerza el rol del teplizumab como una terapia modificadora de la enfermedad en etapas tempranas de la diabetes tipo 1
Diabetes tipo 1 en estadio 2: el rol del teplizumab
Fuente
Karakus KE, Chesshir L, Walker S, et al. Teplizumab treatment for stage 2 type 1 diabetes: a real-world evaluation of metabolic and immunological outcomes. Diabetologia 2026.