Estudio que explora si los biomarcadores de inflamación sistémica de rutina se correlacionan con la resistencia a la insulina en personas con diabetes tipo 2 y su utilidad diagnóstica clínica
Lugones Editorial©
La resistencia a la insulina (IR) es un componente fisiopatológico central de la diabetes tipo 2 (DM2) y se encuentra estrechamente vinculada con un estado de inflamación sistémica crónica de bajo grado. Aunque diversos biomarcadores inflamatorios derivados de análisis de laboratorio de rutina podrían reflejar este entorno inflamatorio-metabólico, su utilidad clínica como indicadores de IR no está completamente establecida.
Con el objetivo de abordar esta cuestión, Jiang et al. realizaron un estudio transversal retrospectivo que incluyó a 2.177 pacientes con DM2 y 327 controles sanos emparejados por edad y sexo, para evaluar la asociación entre marcadores inflamatorios sistémicos disponibles de forma rutinaria y la presencia de resistencia a la insulina.
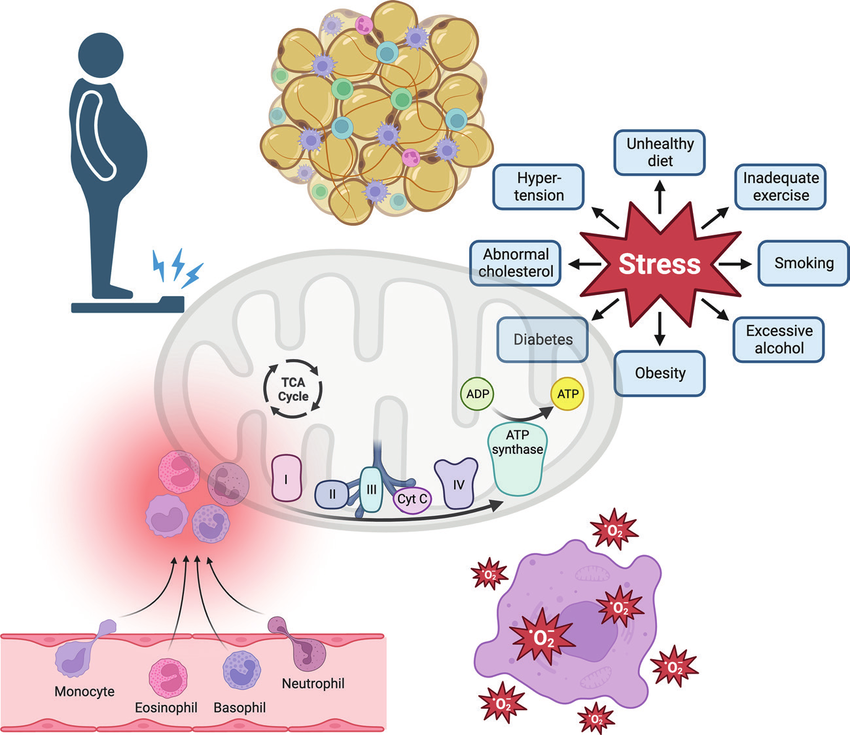
La inflamación crónica de bajo grado ha emergido como un mecanismo biológico estrechamente relacionado con la resistencia a la insulina (Imagen: inflamación crónica de bajo grado y enfermedades crónicas)
Introducción
La IR precede con frecuencia al desarrollo de hiperglucemia manifiesta y constituye un evento temprano clave en la progresión hacia la DM2. En etapas iniciales, la hiperinsulinemia compensatoria mantiene la normoglucemia, pero el estrés metabólico sostenido conduce gradualmente a disfunción de las células β y diabetes establecida. Además, la IR se asocia con dislipidemia, aumento de la adiposidad y mayor riesgo cardiovascular.
En este contexto, la inflamación crónica de bajo grado ha emergido como un mecanismo biológico estrechamente relacionado con la IR. Diversos índices inflamatorios sistémicos -como la relación neutrófilo/linfocito, la relación plaqueta/linfocito, el índice de inflamación inmune sistémica y la proteína C reactiva- han demostrado utilidad en otros escenarios clínicos; sin embargo, su papel en los trastornos metabólicos ha sido menos explorado.
Dado que los métodos de referencia para evaluar IR no son fácilmente aplicables en la práctica clínica rutinaria, identificar biomarcadores simples, accesibles y de bajo costo podría tener relevancia diagnóstica y práctica.
En este marco, el estudio evaluó si los marcadores inflamatorios sistémicos se asocian con IR en personas con DM2 y examinó su capacidad discriminativa, reconociendo las limitaciones inherentes a su diseño transversal.
Métodos
Estudio observacional retrospectivo realizado en el Hospital Zhujiang. Se identificaron inicialmente 2.177 adultos con DM2.
Como grupo de comparación, se incluyeron 327 individuos sanos sin DM, emparejados por edad y sexo, reclutados entre quienes realizaban controles de salud en la misma institución y sin antecedentes inflamatorios, metabólicos o malignos relevantes.
Se obtuvieron de los registros electrónicos datos demográficos y clínicos, incluidos edad, sexo, tabaquismo, comorbilidades, antecedentes familiares y uso de medicación.
El objetivo del presente estudio fue aclarar la posible relevancia clínica de los marcadores inflamatorios disponibles de forma rutinaria como correlatos de la resistencia a la insulina
- Mediciones clínicas y de laboratorio
Las evaluaciones se realizaron tras ayuno nocturno ≥ 12 horas. Se midieron hemograma completo, perfil lipídico (colesterol total, HDL, LDL, triglicéridos), proteína C reactiva ultrasensible (PCR-us), glucosa, hemoglobina glucosilada e insulina en ayunas. Se calculó la relación neutrófilos/linfocitos (NLR) a partir de recuentos absolutos. El recuento de leucocitos se consideró como marcador adicional de inflamación sistémica.
- Definición de resistencia a la insulina
La resistencia a la insulina (IR) se estimó mediante el índice HOMA-IR: insulina en ayunas (mIU/L) × glucosa en ayunas (mmol/L) / 22,5.
Según el consenso chino 2022 sobre IR, los pacientes con DM2 se clasificaron en:
. Grupo con IR: HOMA-IR ≥ 2,80
. Grupo sin IR: HOMA-IR < 2,80
Los individuos sanos constituyeron el grupo control.
Resultados
Se analizaron tres grupos: pacientes con DM2 con resistencia a la insulina (IR), pacientes con DM2 sin IR y controles sanos. Los grupos fueron comparables en edad, sexo y tabaquismo. La presión arterial no mostró diferencias significativas y se incluyó únicamente con fines descriptivos.
El índice de masa corporal (IMC) fue significativamente mayor en el grupo con IR, reforzando la estrecha asociación entre adiposidad y resistencia a la insulina.
- Comparación entre DM2 y controles sanos
En comparación con los controles, los pacientes con DM2 presentaron mayor glucosa en ayunas, HbA1c, insulina y HOMA-IR, confirmando el deterioro glucémico esperado.
En el perfil lipídico, solo los triglicéridos estuvieron significativamente elevados en DM2; colesterol total, HDL y LDL no difirieron, lo que sugiere una alteración lipídica selectiva.
Los marcadores de inflamación sistémica (PCR-us, leucocitos y NLR) fueron significativamente más altos en DM2. El aumento del NLR se explicó principalmente por mayor recuento de neutrófilos, sin diferencias relevantes en linfocitos absolutos.

La inflamación sistémica de bajo grado está estrechamente ligada a la resistencia a la insulina en diabetes tipo 2
- DM2 según estado de resistencia a la insulina
Dentro de la cohorte con DM2, los pacientes con IR mostraron un perfil metabólico más desfavorable: mayores triglicéridos, colesterol total, LDL, glucosa, HbA1c, insulina y HOMA-IR, y menor HDL.
También presentaron mayores niveles de PCR-us, leucocitos y NLR, acompañados de neutrofilia y leve reducción de linfocitos, configurando un perfil proinflamatorio asociado a menor sensibilidad insulínica.
- Asociación entre inflamación sistémica y resistencia a la insulina
El análisis de correlación de Spearman mostró asociaciones positivas significativas entre HOMA-IR y todos los marcadores inflamatorios evaluados.
La relación neutrófilos/linfocitos (NLR) presentó la correlación más fuerte, seguida por leucocitos y PCR-us, lo que sugiere que los índices celulares reflejan de manera consistente la carga inflamatoria vinculada a la IR.
- Análisis multivariable
En la regresión logística ajustada por variables demográficas y metabólicas, el NLR permaneció independientemente asociado con la IR, junto con IMC, HbA1c y triglicéridos.
En cambio, PCR-us y leucocitos perdieron significación tras el ajuste, lo que sugiere que el NLR podría captar dimensiones inflamatorias más estrechamente vinculadas a la resistencia insulínica.
- Rendimiento discriminatorio
En el análisis ROC, el NLR mostró el mayor AUC entre los marcadores inflamatorios, con mayor sensibilidad, pero menor especificidad en comparación con PCR-us y leucocitos.
No obstante, el desempeño global fue modesto, por lo que el NLR no debe considerarse un marcador diagnóstico independiente de IR, aunque podría aportar información complementaria en la práctica clínica.
El NLR mostró la mayor área bajo la curva entre los marcadores estudiados, con sensibilidad relativamente alta, pero especificidad baja, lo que sugiere que puede ser útil como marcador complementario, pero no como prueba diagnóstica independiente
Discusión
Este estudio demuestra que los marcadores de inflamación sistémica -en particular la relación neutrófilos/linfocitos (NLR), la PCR-us y el recuento leucocitario- se encuentran progresivamente elevados desde controles sanos hasta pacientes con DM2 sin resistencia a la insulina (IR) y, en mayor medida, en aquellos con IR. Esta gradiente inflamatoria refuerza la estrecha asociación entre inflamación crónica de bajo grado y deterioro metabólico.
Todos los marcadores se correlacionaron positivamente con HOMA-IR, siendo la NLR la que mostró la asociación más fuerte, lo que sugiere que los índices celulares podrían reflejar con mayor sensibilidad el componente inflamatorio de la resistencia insulínica.
- NLR como marcador inflamatorio integrado
Los pacientes con IR presentaron neutrofilia relativa y leve reducción linfocitaria, configurando un NLR elevado. Este patrón es consistente con un predominio de inmunidad innata proinflamatoria, fenómeno descrito en estados metabólicos adversos.
En los modelos multivariables, la NLR permaneció independientemente asociada con IR aun tras ajustar por IMC, HbA1c y triglicéridos. Este hallazgo constituye uno de los aportes centrales del estudio: la NLR aporta información inflamatoria no completamente explicada por los parámetros metabólicos clásicos.
Desde el punto de vista biológico, la hiperglucemia y la dislipidemia favorecen activación neutrofílica, estrés oxidativo y liberación de mediadores inflamatorios que interfieren con la señalización insulínica. En paralelo, la linfopenia relativa podría reflejar alteraciones adaptativas en un entorno inflamatorio crónico.
- Valor clínico y limitaciones diagnósticas
En el análisis ROC, la NLR mostró el mayor AUC (≈0,67) y mayor sensibilidad que la PCR-us y el recuento leucocitario, aunque con especificidad menor y rendimiento global modesto. Por lo tanto, no se propone como herramienta diagnóstica independiente de IR, sino como marcador complementario, accesible y de bajo costo.
El mejor desempeño de la NLR respecto a la PCR-us podría explicarse porque esta última refleja principalmente respuesta hepática de fase aguda, mientras que la NLR capta dinámicamente cambios en poblaciones celulares inmunes, potencialmente más sensibles al estado inflamatorio metabólico crónico.
Lo novedoso radica en demostrar, en una cohorte amplia de más de 2.000 pacientes con DM2, que la NLR se asocia de manera independiente con la resistencia a la insulina y supera a marcadores inflamatorios clásicos en su correlación con HOMA-IR. Esto posiciona a la NLR como un posible indicador clínico complementario dentro del eje inflamación sistémica–diabetes.
No obstante, el diseño transversal impide establecer causalidad y las asociaciones deben interpretarse como coexistencia inflamatorio-metabólica.

En personas con diabetes tipo 2, los marcadores de inflamación sistémica se asocian positivamente con la resistencia a la insulina, siendo la NLR el índice con mayor correlación y asociación independiente
Conclusiones
En personas con diabetes tipo 2, los marcadores de inflamación sistémica se asocian positivamente con la resistencia a la insulina, siendo la NLR el índice con mayor correlación y asociación independiente.
Si bien su capacidad discriminativa es modesta, la NLR -derivada de un hemograma de rutina- podría considerarse un marcador complementario de riesgo inflamatorio-metabólico en DM2, más que una herramienta diagnóstica autónoma.
Se requieren estudios prospectivos y longitudinales para determinar la direccionalidad de la relación inflamación–IR y evaluar si la modificación de la inflamación sistémica, incluida la inducida por terapias antidiabéticas con efectos antiinflamatorios, se traduce en mejoras sostenidas de la sensibilidad insulínica.
Inflamación sistémica y diabetes
Fuente
Jiang Y, Yan M, Li H, et al. Correlation between systemic inflammation markers and insulin resistance in type 2 diabetes mellitus patients and its diagnostic value análisis. Front. Med. 2026;12.









