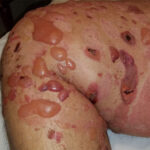
Las enfermedades ampollares subepidérmicas autoinmunes constituyen un grupo heterogéneo con superposición clínica, histológica e inmunológica; en este trabajo se intenta clarificar conceptos y brindar claves diagnósticas
Lugones Editorial©
Existe una gran superposición clínica, histológica e inmunológica entre las enfermedades ampollares subepidérmicas autoinmunes (EASA). El conocimiento molecular de la unión dermoepidérmica es básico para comprender este grupo de patologías.
Los estudios inmunológicos son absolutamente imprescindibles para el diagnóstico de este grupo heterogéneo de enfermedades; a pesar de ello, no ha hecho más que incrementar la sensación de inmenso desconocimiento que se tiene cuando se profundiza acerca de las EASA. En la práctica ocurre que casos clínicamente sospechosos de un tipo de EASA se corresponden inmunológicamente con otro.
En este trabajo, los autores intentan clarificar algunos conceptos y brindar claves diagnósticas.
| Denominación | Clases de inmunoglobulinas y/o complemento | Autoantígenos | |
| Penfigoides y sus variantes | |||
| Penfigoide ampollar (PA) arquetípico | IgG | BP230, BP180 (dominio NC16a) | |
| PA localizado | IgG, C3 | BP180 | |
| PA nodular | IgG, C3 | BP180, etc. | |
| PA vegetante | IgG, C3 | BP180, etc. | |
| PA eccema like | IgG, C3 | BP180, etc. | |
| PA vesicular | IgG, C3 | BP180, etc. | |
| PA dishidriforme | IgG, C3 | BP180, etc. | |
| PA inducido por drogas | IgG, C3 | BP180 | |
| Liquen plano penfigoide | IgG, C3 | BP230, BP180 (dominio NC16a) | |
| PA antilaminina p200 | IgG, C3 | Cadena de 200kD de las lamininas | |
| Penfigoide gestacional (antes herpes gestacional) | IgG | BP180 (dominio NC16a) | |
| Penfigoides de las mucosas (PMM) y subtipos | |||
| Por el blanco antigénico | PMM anti-180 | IgG, C3, IgA | BP180 (dominio terminal) |
| PMM antilaminina 332 | IgG | Laminina 332 | |
| PMM anti-p200 | IgA/IgG | p200 (laminina cadena γ1) | |
| Por la clínica | PMM ocular puro | IgG, IgA,C3 | Integrina 332 cadena β4 |
| PMM oral | IgG, IgA,C3 | Integrina 332 cadena α6 | |
| Epidermólisis ampollar adquirida | IgG, C3 | Colágeno VII (fibras de anclaje) | |
| Lupus eritematoso ampollar | IgG,C3 | Colágeno VII (fibras de anclaje) | |
| Dermatosis a IgA lineal | |||
| Tipo lámina lúcida | IgA,C3 | BP180 (97/120kD) | |
| Tipo sublámina densa | IgA,C3 | Colágeno VII | |
| Dermatitis herpetiforme | IgA granular, C3 | eTg3, Tg2 (endomisio) | |
Enfermedades ampollares autoinmunes dermoepidérmicas. Clases de inmunoglobulinas y autoantígenos de las enfermedades penfigoides
Introducción
Este grupo heterogéneo de enfermedades ampollares subepidérmicas autoinmunes (EASA) clínicamente se caracteriza por ampollas tensas; de estas, la más frecuente el penfigoide ampollar (PA), pero con semejanzas clínicas e histológicas con otras entidades.
La zona de la membrana basal (ZMB) es una estructura molecular compleja, formada por los queratinocitos basales, la membrana basal epidérmica y los ápices de las papilas dérmicas. Es una zona altamente especializada, con múltiples funciones, y la adhesión entra la epidermis y la dermis es una de ellas. Este cometido se altera cuando se produce una respuesta autoinmune con autoanticuerpos (aAcs) contra determinadas moléculas de la ZMB lo que da como resultado la formación de ampollas por despegamiento dermoepidérmico.
Entre estas superposiciones clínicas, histológicas e inmunológicas que se atribuyen a la expansión de epítopo, existe la exposición de un determinado antígeno previamente “secuestrado” que responde con una respuesta autoinmune. Los estudios inmunológicos resultan hoy en día absolutamente imprescindibles para el diagnóstico de este grupo de enfermedades.
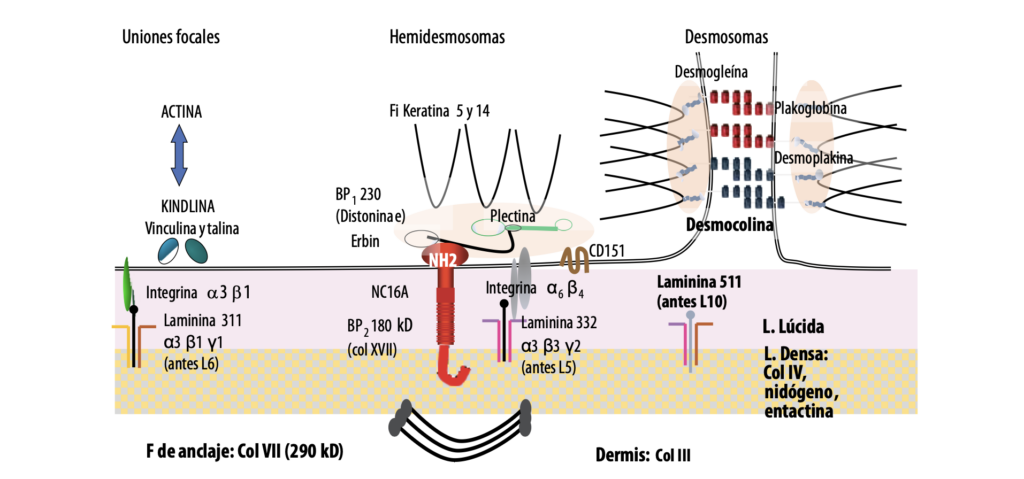
Esquema de la zona membrana basal
Métodos diagnósticos
Los objetivos en el diagnóstico de las EASA son: 1) distinguir las EASA de otras enfermedades ampollares hereditarias, infecciosas o por otros mecanismos inmunológicos; 2) diferenciarlas entre ellas; 3) monitorizar el curso, detectar brotes y ajustar el tratamiento.
- Histopatología
La biopsia para hematoxilina eosina (HE) se coloca en formol 10% y debe realizarse en el borde de la ampolla para visualizar el sitio de despegamiento. Se aconseja no biopsiar ampollas enteras. En la histopatología (HP), el despegamiento subepidérmico presenta una ampolla cuyo techo es la epidermis y el piso, la dermis. El infiltrado inflamatorio es de leucocitos polimorfonucleares (PMN) y pueden predominar los neutrófilos o eosinófilos.
- Inmunohistoquímica
Se puede realizar una tinción de alguna proteína conocida y visualizar el sitio de despegamiento patológico. El colágeno IV es el más utilizado; se ubica entre el colágeno VII y la laminina, y permite diferenciar entre la epidermólisis ampollar adquirida (EAA) y el penfigoide anti-p200. La ventaja de este método es que puede realizarse en muestras ya fijadas en formol
- Inmunofluorescencia
El objetivo de la inmunofluorescencia (IF) es detectar la presencia de aAcs en la ZMB.
Detección de depósitos autoinmunes en la piel
- Inmunofluorescencia directa
La inmunofluorescencia directa (IFD) permite detectar los depósitos de inmunorreactantes (IgG, IgM, IgA y C3) y determinar si es epidémica, en la zona de la membrana basal, o dérmica con un patrón de disposición lineal o granular.
La elección del sitio de la toma de la biopsia es clave para el diagnóstico. La misma debe realizarse perilesional con un punch de biopsia inferior a 3 mm. El sitio de la toma también puede influir, siendo por ejemplo poco aconsejable la toma de las piernas para el PA y elegir las áreas menos traumáticas en el penfigoide de las membranas mucosas (PMM).
La muestra se coloca en solución fisiológica y se transporta en frío entre 4 a 0 ºC. Una vez en el laboratorio, la muestra se corta en criostato intentando que los cortes no superen los 4 µm de grosor; luego son cubiertos con una solución que contiene anticuerpos (Acs) anti-inmunoglobulinas humanas marcados con fluorocromos. El más usado es el isotiocianato de fluoresceína (FITC) que emite fluorescencia verde y, en segundo lugar, la rodamina de color rojo.
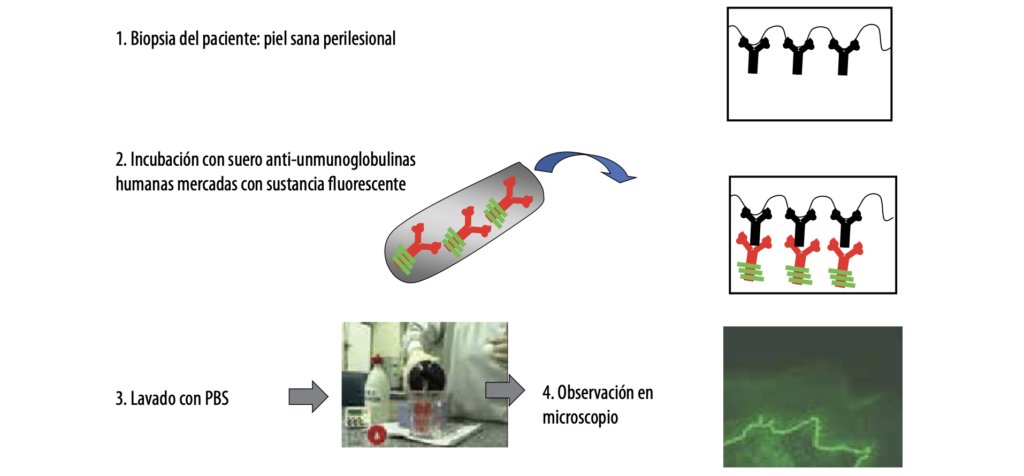
Esquema de la técnica de inmunofluorescencia directa
Técnica de salt-split
Permite la separación dermoepidérmica. La biopsia se coloca en un envase con cloruro de sodio 1 molar frío durante 48 a 72 horas (incubación). Esta solución provoca la separación (clivaje) dermoepidérmica a nivel de la lámina lúcida.
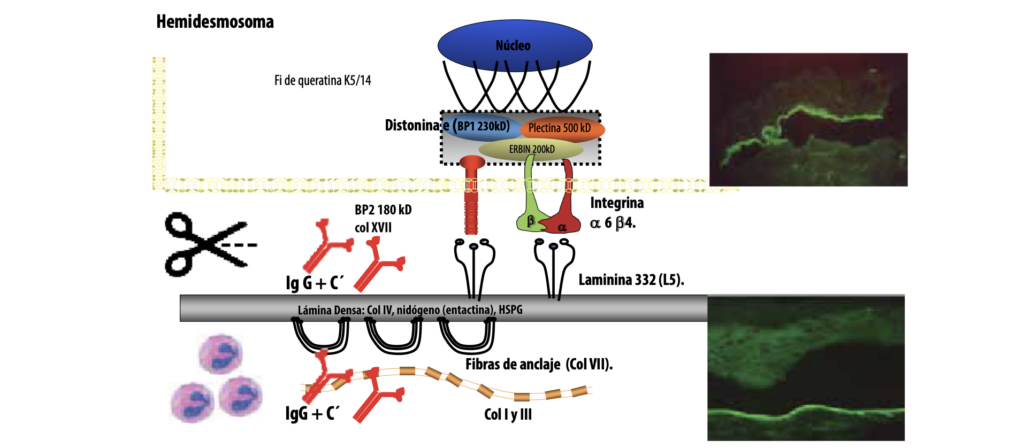
Esquema de inmunofluorescencia con técnica de salt-split.
Técnicas para detectar anticuerpos en suero u otros fluidos
- Inmunofluorescencia indirecta
La inmunofluorescencia indirecta (IFI) detecta los Acs circulantes y permite estimar su concentración mediante diluciones seriadas. Se utilizan diferentes sustratos antigénicos (piel humana clínicamente sana, esófago de mono, esófago de conejo, etc.).
Se extraen de 5 a 10 ml de sangre venosa del paciente y luego se separa el suero el cual se vierte sobre el sustrato (tejido con epitelio plano estratificado) dejándolo aproximadamente 30 minutos (incubación). Después del lavado en buffer salino (PBS), se incuba con anti-inmunoglobulina humana marcada con un fluorocromo (segunda incubación), se vuelve a lavar en PBS, se seca y, por último, se procede a su observación en un microscopio con lámpara fluorescente.
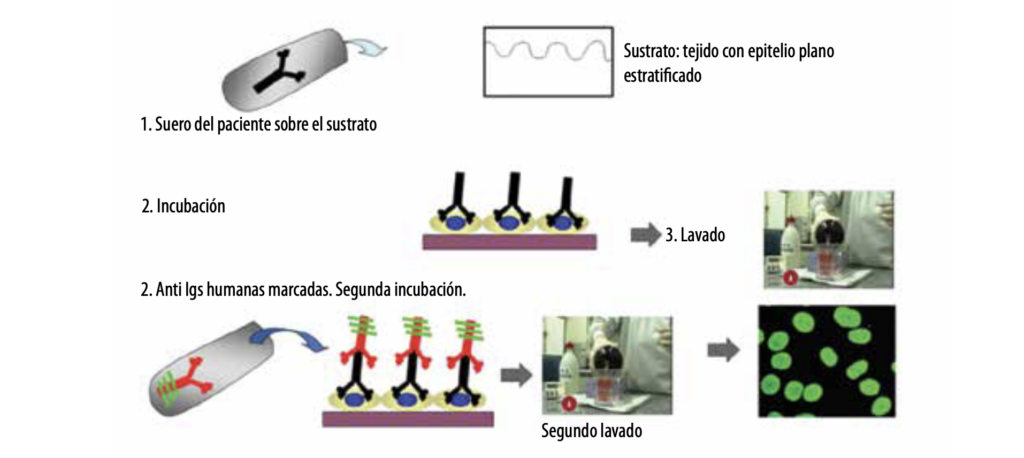
Esquema de técnica de inmunofluorescencia indirecta
- Patrones dentados en U o N en cortes finos
En ocasiones, cuando se emplean cortes muy finos, en la IFI se puede observar que los depósitos en la ZMB tienen un aspecto dentado o serrado que se puede notar como una letra “N” o “U”.
El patrón dentado tipo N se observa cuando la ampolla se originó por encima de la lámina densa por aAcs contra componentes del hemidesmosoma, p. ej., PA, penfigoide gestacional, algunos penfigoides de las mucosas, penfigoide anti-p200 y penfigoide antilaminina 332, y el patrón serrado en U en enfermedades donde el autoanticuerpo se une a antígenos (Ags) ubicados en la sublámina, como aAcs contra el colágeno VII (COL7) de la EAA y lupus eritematoso sistémico ampollar (LESA).
- Ensayo por inmunoadsorción ligada a enzimas
La prueba de ELISA es un método práctico y de fácil realización, pero no presenta resultados concluyentes para las enfermedades de la ZMB, lo que plantea la necesidad de utilizar las técnicas de inmunotransferencia en los casos de mayor dificultad diagnóstica.
La prueba de ELISA disponible actualmente permite detectar cinco moléculas: desmogleína 1 y 3, BP180, BP230 y colágeno VII.
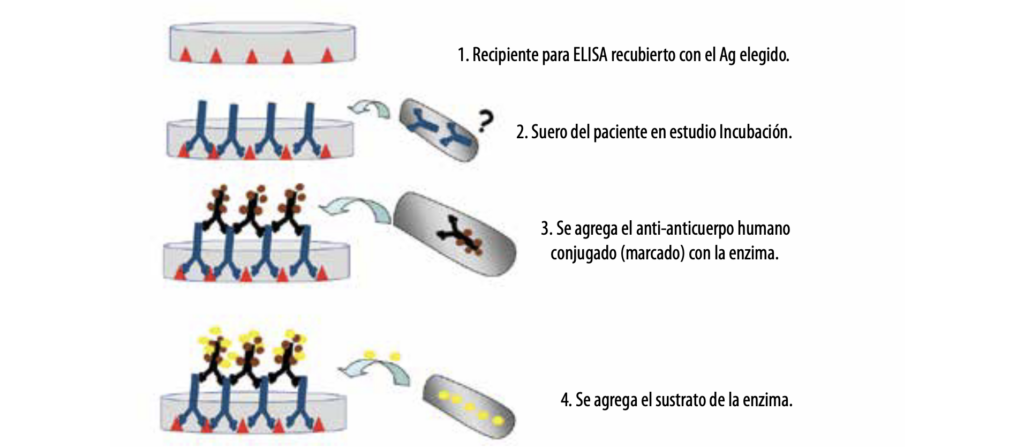
Esquema de técnica de ELISA
- Inmunotransferencia o electroinmunotransferencia (Western blot)
Con esta técnica, en el estudio de pacientes con EASA, las proteínas que forman parte del epitelio plano estratificado y la ZMB se separan por su peso y transfieren a un soporte sólido para luego enfrentarlas al suero del paciente y determinar si tiene Acs contra alguna de ellas.
La desventaja del inmunoblot es que al tener que desnaturalizar las proteínas, se pierden puntos de unión antígeno-anticuerpo denominados epítopos conformacionales. Esta técnica tiene una baja sensibilidad y aumenta el número de falsos negativos.
- Inmunoprecipitación
Esta técnica no desnaturaliza las proteínas, pero es más compleja y lenta que el inmunoblot y, por lo tanto, se usa fundamentalmente para investigación.
- Microscopia electrónica
Es una técnica lenta y complicada que no aporta ventajas en el diagnóstico de las EASA porque no brinda información sobre la composición de los depósitos autoinmunes.
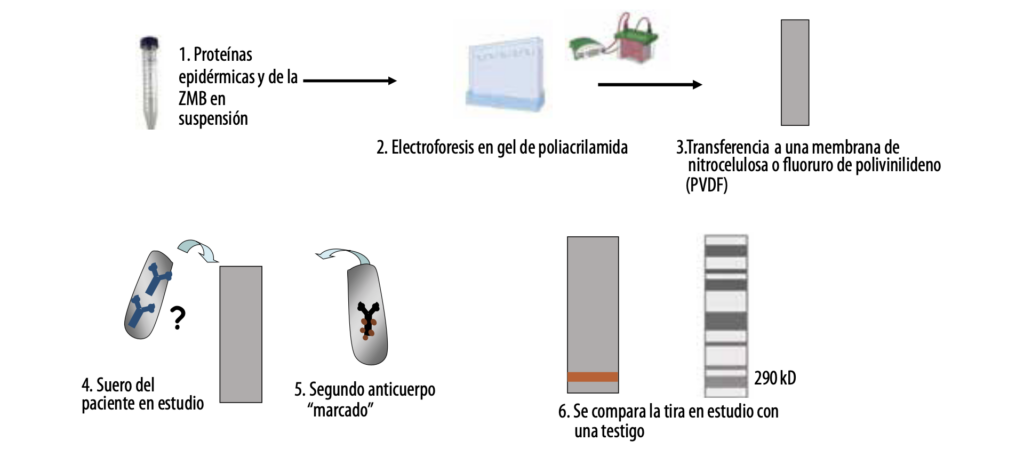
Esquema de técnica de Western blot
Penfigoide ampollar
El PA es el más frecuente de las EASA. En la HP la ampolla subepidérmica se acompaña de infiltrado inflamatorio con predominio eosinofílico. La IFD es el gold standard y el primer paso para el diagnóstico; evidencia depósitos lineales de IgG y C3 en la ZMB en aproximadamente el 90% de los pacientes. Los falsos negativos pueden darse por niveles de Acs no detectables en los inicios de la patología, presentación de otros antígenos, no reactivos al anti-IgG y también en pacientes con otra subclase de IgG. Cuando la sospecha clínica es alta, se aconseja repetir una segunda biopsia.
Con la técnica de salt-split, los aAcs se unen al techo (lado epidérmico) de esta ampolla, sitio donde se ubican sus blancos antigénicos. Este hallazgo es útil para diferenciarlo de otras entidades de la ZMB, como la EAA donde los Acs impactan en la base (lado dérmico) de la ampolla.
Con técnicas de inmunohistoquímica contra el colágeno IV y la laminina se puede observar que estos componentes se encuentran en el piso de la ampolla.
La IFI es positiva en aproximadamente un 70% de los casos. Generalmente, entre un 60-80% son IgG, con menor frecuencia IgA e IgE. Los Acs IgE dirigidos a BP230 se pueden identificar en 38-68% de los pacientes con PA, sin embargo, el valor diagnóstico y patogénico de la IgE anti-BP230 aún no es concluyente.
El Ag principal del PA es el BP180. La mayoría de los aAcs se dirige al dominio no colagenasa 16a del mismo (BP180 NC16a).
El papel patogénico de los Acs contra BP180 en esta entidad está ampliamente demostrado; sin embargo, el de los Acs contra BP230 no está del todo dilucidado y se postula que aparecerían como resultado del fenómeno de dispersión de epítopos.
Los kit comerciales de ELISA detectan BP180 NC16a y 230. Esta técnica no sería utilizada como la única herramienta ya que su sensibilidad es del 54% para BP180 y del 48% para BP230. Combinados, la misma aumenta al 66%. La especificidad se ubica en un 94% para BP180 y en un 89% para BP230.
La técnica de inmunoblot tiene una sensibilidad del 60-100% mayormente dirigido a BP180, pero la especificidad es muy baja por lo que no se recomienda para su diagnóstico.
Penfigoide gestacional
El penfigoide gestacional (PG) ocurre en el embarazo por una reacción cruzada de los aAcs de la clase IgG contra BP180 placentarios, específicamente el dominio NC16a, y rara vez a los BP230. Ocurre durante el segundo o tercer trimestre del embarazo, con remisión completa luego del parto. Las lesiones urticarianas y las ampollas subepidérmicas se caracterizan en la HP por un marcado edema papilar e infiltrado inflamatorio con abundantes eosinófilos.
La IFD es el gold standard y muestra depósito lineal de C3 en la ZMB en aproximadamente el 100% de los casos, y algo menor para IgG. La IFI, ELISA e inmunoblot son menos sensibles y específicos de acuerdo a varias series estudiadas.
Liquen plano penfigoide
El liquen plano penfigoide (LPP) se caracteriza por ampollas tensas y liquen plano (LP). El mecanismo de formación de la ampolla es por aAcs dirigidos contra el BP180 a diferencia del liquen plano ampollar que es por degeneración hidrópica (inmunidad celular).
La HP muestra el despegamiento subepidérmico con infiltrado inflamatorio con eosinófilos, y en las lesiones de LP, acantosis irregular en “dientes de sierra”, degeneración vacuolar, presencia de células apoptóticas, e infiltrado subepidérmico en banda compuesto por linfocitos e histiocitos (característico del LP).
La IFD permite detectar, en las muestras obtenidas de piel sana perilesional de ampollas, depósitos lineales de IgG y C3. Con la técnica de salt-split, los aAcs se unen en el techo y con la técnica de ELISA en suero del paciente se detectan anti-BP180. En tanto que en las muestras de pápulas de liquen plano, se observan acúmulos globulares de IgM característicos de las reacciones liquenoides.
Penfigoide de las mucosas
El penfigoide de las mucosas (PMM; antes llamado, cicatrizal o mucosinequiante) representa un grupo heterogéneo de enfermedades ampollares autoinmunes inflamatorias y crónicas, que compromete principalmente las mucosas (oral, ocular, faríngea, nasal, esofágica, laríngea y anogenital) y, con menor frecuencia, la piel, con tendencia a la formación de cicatrices.
Ante la sospecha clínica es necesario el estudio histopatológico y la IFD para arribar al diagnóstico. En la HP las ampollas subepidérmicas se encuentran asociadas a un infiltrado variable. Al inicio predominan los neutrófilos, incluso en microabscesos papilares; posteriormente los eosinófilos y en las lesiones más antiguas, linfocitos y lesiones cicatrizales en la dermis.
La IFD detecta el depósito lineal IgG, IgA y/o C3 en la ZMB. En un alto porcentaje es negativa, sobre todo cuando la localización es ocular, siendo menester repetirla. La IFI detecta aAcs en un bajo porcentaje de los pacientes. Con la técnica de salt-split, la fluorescencia puede ser en el techo, en el piso o en ambos, según los blancos antigénicos involucrados (BP180, BP230, laminina 332, integrina α6 β4, colágeno VII, entre otros). Los kit de ELISA comercialmente disponibles en la actualidad detectan solo algunos de los Ags involucrados en el PMM, siendo complementaria de la IF.
Con inmunoblot se puede detectar el aAc anti-laminina 332, pero no con ELISA.
Epidermólisis ampollar adquirida
La epidermólisis ampollar adquirida (EAA) es una rara enfermedad ampollar subepidérmica y crónica, caracterizada por aAcs dirigidos al colágeno VII. En la HP podemos observar la ampolla subepidérmica, con o sin infiltrado a predominio neutrofílico.
La IFD presenta depósitos de IgG y/o C3 con patrón lineal en la ZMB, a veces puede haber IgA y/o IgM. Con cortes finos, se pueden observar patrones en U o dientes de sierra, como se mencionó anteriormente. La IFI muestra depósitos de IgG a títulos bajos. Con la técnica de salt-split, los inmunorreactantes impactan del lado dérmico (piso).
Con técnicas de inmunohistoquímica contra el colágeno IV y la laminina, estos se ubican en el techo de la ampolla. Con ELISA, la reactividad es al colágeno VII.
Lupus eritematoso sistémico ampollar
El lupus eritematoso sistémico ampollar (LESA) es una manifestación infrecuente del lupus eritematoso sistémico (LES) causada por aAcs contra el colágeno VII y otros componentes de la ZMB. Los pacientes deben cumplir criterios de LES.
La HP presenta ampollas subepidérmicas con infiltrado a predominio neutrofílico. Con tinción de azul alcián se puede observar incremento de mucina.
Todas las técnicas de inmunohistoquímica son indistinguibles de la EAA ya que los aAcs se dirigen contra el mismo blanco: el colágeno VII.
Penfigoide antilaminina p200
Clínicamente puede simular otras dermatosis ampollares autoinmunes. Mediante la IF con técnica de salt-split se observan los inmunorreactantes en el piso de la ampolla (lado dérmico).
El diagnóstico se confirma mediante inmunoblot, una técnica en la que el suero reacciona contra la proteína de 200 kDa; es compleja y poco accesible, no disponible en la Argentina. Se puede realizar inmunohistoquímica marcando el colágeno IV; es un procedimiento sencillo y disponible que se realiza sobre tacos de biopsia. Se observa la tinción en el suelo de la ampolla diferenciándolo de la EAA y del LESA, que lo hace en el techo.
Dermatosis a IgA lineal
En la HP se observa la ampolla subepidérmica con infiltrado de neutrófilos en la dermis papilar. La IFD detecta depósitos de IgA con disposición lineal siguiendo la ZMB y debe solicitarse la técnica de salt-split; se puede observar depósito epidérmico (techo) que es más frecuente, o dérmico (piso) o en ambos, debido a su heterogeneidad antigénica. La mayoría de los pacientes con dermatosis a IgA lineal (DIAL) desarrolla aAcs de tipo IgA contra BP180 (o BPAg2). La región NC16a es el sitio inmunodominante, con mayor cantidad de epítopos. Hay otros Ags involucrados: laminina 331 cadena γ 1, BPAG1 o BP230, LAD-285, colágeno VII.
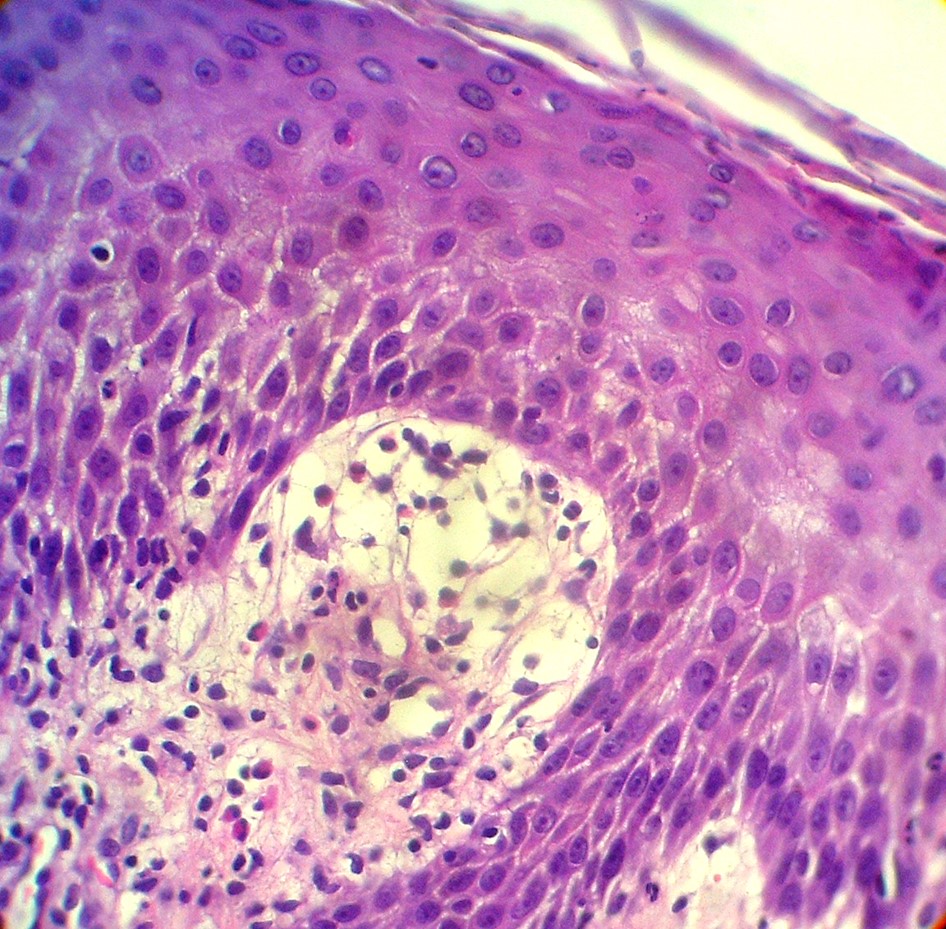
Ampolla subepidérmica con infiltrado eosinofílico (HyE, 40X).
Dermatitis herpetiforme
La dermatitis herpetiforme (DH) es una enfermedad ampollar autoinmune causada por la reacción autoinmune al gluten. En la HP es característico el infiltrado de neutrófilos en los vértices de las papilas y la ampolla por despegamiento dermoepidérmico. La IFD muestra un patrón granular de IgA en la dermis papilar, siendo patognomónico. Tiene una sensibilidad y especificidad del 90%.
Las serologías solicitadas son aAc IgA antitransglutaminasa tisular (anti-TGt o Tg2) por ELISA, y aAc IgA antiendomisio por IFI usando como sustrato esófago de mono y aAc antipéptidos deamidados de la gliadina (PDG).
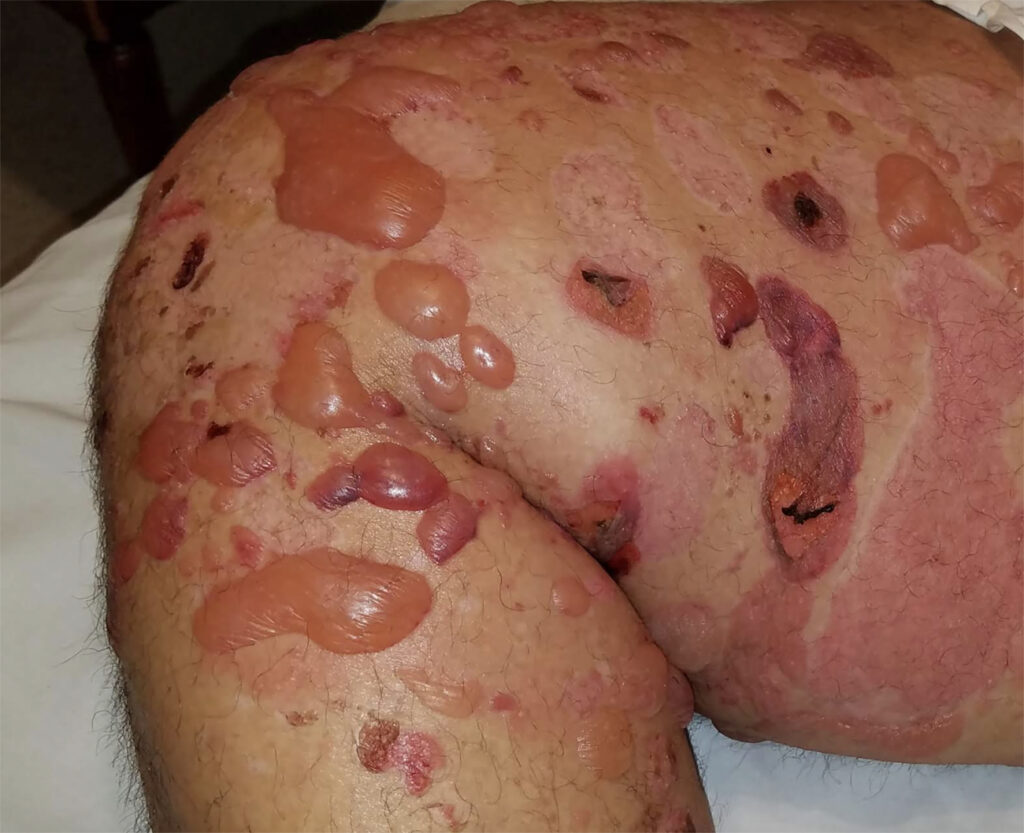
Ampollas tensas con contenido citrino
Conclusiones
Las enfermedades ampollares autoinmunes son un grupo complejo de patologías. Por la similitud clínico-patológica, actualmente se aconseja fuertemente pedir los estudios complementarios que correspondan a fin de arribar a un diagnóstico certero y brindar el tratamiento más apropiado.
Enfermedades ampollares subepidérmicas autoinmunes
Fuente
Di Milia MB, Label MG, Cabral Campana L. Diagnóstico de enfermedades ampollares subepidérmicas autoinmunes. Dermatol Argent 2024;30(1):2-10.