Una microbiota cutánea equilibrada es esencial para la salud. Se revisan los productos basados en el microbioma y su potencial terapéutico en enfermedades inflamatorias de la piel
Lugones Editorial©
A diferencia de las terapias convencionales que a menudo interrumpen la microbiota y conducen a efectos secundarios o resistencia, los productos basados en microbioma ofrecen una estrategia más específica para prevenir y controlar enfermedades inflamatorias de la piel.
Estos productos, que incluyen probióticos, prebióticos, postbióticos y agentes bioterapéuticos vivos, están diseñados para modular el ecosistema de la piel mejorando las poblaciones microbianas beneficiosas, suprimiendo las cepas patógenas y mejorando la tolerancia inmune.

Los nuevos enfoques terapéuticos se orientarán a restaurar el equilibrio microbiano y promover la salud de la piel a través de intervenciones basadas en el microbioma
Mantener una microbiota cutánea equilibrada es esencial para la salud de la piel, mientras que las interrupciones en la composición de la microbiota de la piel, conocidas como disbiosis, pueden contribuir al inicio y la progresión de varios trastornos de la piel.
La disbiosis microbiota se ha asociado con varias afecciones inflamatorias de la piel, incluyendo dermatitis atópica, dermatitis seborreica, acné, psoriasis y rosácea. Los recientes avances en la secuenciación de alto rendimiento y los análisis metagenómicos han proporcionado una comprensión más profunda de las comunidades microbianas de la piel tanto en la salud como en la enfermedad.
Estos descubrimientos se están traduciendo ahora en nuevos enfoques terapéuticos destinados a restaurar el equilibrio microbiano y promover la salud de la piel a través de intervenciones basadas en el microbioma.
La disbiosis microbiota se ha asociado con varias afecciones inflamatorias de la piel, incluyendo dermatitis atópica, dermatitis seborreica, acné, psoriasis y rosácea
Disbiosis de la microbiota cutánea y enfermedades inflamatorias de la piel
El equilibrio de la microbiota cutánea es fundamental para la protección frente a enfermedades de la piel.
Diversas enfermedades inflamatorias crónicas, como dermatitis atópica, dermatitis seborreica, acné, psoriasis y rosácea, se asocian con disbiosis, generalmente caracterizada por un aumento de Staphylococcus aureus y una disminución de Cutibacterium. Cada enfermedad presenta un perfil microbiano particular, con alteraciones específicas que definen su disbiosis.
Más allá de la piel, la hipótesis del eje intestino-piel propone que la interacción entre el sistema inmunológico, las vías metabólicas y hormonales, y el sistema nervioso vincula la salud gastrointestinal con la cutánea.
La microbiota intestinal modula la inmunidad, y su desequilibrio puede afectar la piel. Según esta hipótesis, las afecciones inflamatorias cutáneas resultan de la interacción compleja entre genética, estilo de vida y sistema neuro-inmuno-endocrino, en la que intestino y piel interactúan continuamente a través de sus microbiotas. La coexistencia de enfermedades cutáneas e intestinales respalda esta interdependencia.
Dermatitis atópica
La fisiopatología de la dermatitis atópica (DA) se explica mediante dos hipótesis: la externa, que atribuye la enfermedad a un defecto de la barrera cutánea que facilita la penetración de alérgenos e induce inflamación, y la interna, que plantea un defecto inmunológico primario que provoca disfunción de la barrera, disbiosis y mayor susceptibilidad a alérgenos.
En la DA se observa una alteración marcada de la microbiota cutánea, con menor diversidad y disminución de géneros como Cutibacterium, Streptococcus, Acinetobacter, Corynebacterium y Prevotella, acompañada de un aumento significativo de Staphylococcus, especialmente S. aureus. Este aumento es más pronunciado durante brotes graves, donde una sola cepa de S. aureus puede dominar.
La gravedad de la DA también se relaciona con una disminución de estafilococos comensales negativos para la coagulasa, como S. epidermidis y S. hominis, que normalmente protegen la piel mediante péptidos antimicrobianos.
Estudios en recién nacidos muestran que niveles bajos de estafilococos comensales tempranos se asocian con mayor riesgo de desarrollar DA, mientras que la presencia temprana de S. aureus precede al inicio de los síntomas.
En cuanto a los hongos, los estudios son más limitados, pero Malassezia, especialmente M. globosa y M. restricta, predomina también en la DA.
Finalmente, cambios en las comunidades virales también parecen jugar un papel. Los fagos específicos de S. aureusson más abundantes en pacientes con DA, sugiriendo que favorecen el crecimiento de la bacteria, mientras que ciertos fagos podrían ejercer un efecto protector, disminuyendo a medida que la enfermedad se agrava.

Estudios en recién nacidos muestran que niveles bajos de estafilococos comensales tempranos se asocian con mayor riesgo de desarrollar dermatitis atópica
Dermatitis seborreica
La etiología de la dermatitis seborreica (DS) es multifactorial, involucrando respuestas inmunitarias, disbiosis de la microbiota cutánea y aumento de la actividad de los sebocitos.
La microbiota cutánea de pacientes con DS presenta desequilibrio tanto fúngico como bacteriano. Malassezia spp., aunque forma parte de la microbiota normal, contribuye al inicio y la gravedad de la enfermedad mediante producción de lipasas y fosfolipasas que descomponen el sebo, liberando ácidos grasos insaturados y peróxidos lipídicos que provocan inflamación.
Esto activa vías NF-κB y MAPK en queratinocitos, induce la liberación de citoquinas, promueve la proliferación de queratinocitos y engrosamiento del estrato córneo, comprometiendo la barrera cutánea y favoreciendo la invasión fúngica. La presencia de micovirus asociados a Malassezia también se vincula con mayor gravedad de la enfermedad.
La disbiosis bacteriana complementa este proceso. Los ácidos grasos liberados por Malassezia elevan el pH cutáneo, promoviendo el crecimiento y la adhesión de S. aureus, la bacteria más prevalente en piel afectada por DS. En áreas no lesionales predomina Cutibacterium, mientras que en áreas lesionales predominan Staphylococcus, Streptococcus y Acinetobacter.
Esta composición microbiana contribuye a la patogénesis de la enfermedad: niveles elevados de Staphylococcus se asocian con mayor pérdida de agua transepidérmica y aumento del pH, indicando daño de barrera, mientras que Cutibacterium se relaciona con mejor hidratación e integridad de la piel.

La microbiota cutánea de pacientes con dermatitis seborreica presenta desequilibrio tanto fúngico como bacteriano
Acné
Cutibacterium acnes, predominante en áreas sebáceas, está implicado en el desarrollo del acné.
Aunque la abundancia relativa de C. acnes puede ser similar entre individuos con y sin acné, las estructuras de población a nivel de cepa difieren significativamente. El predominio de los filotipos IA1 y IA2 se asocia con la enfermedad, mientras que otras cepas se encuentran en piel sana.
La gravedad del acné se correlaciona con un aumento de Staphylococcus. Sin embargo, estafilococos comensales, como S. epidermidis, desempeñan un papel protector al mantener la homeostasis de C. acnes en la piel sana. S. epidermidis inhibe la proliferación de C. acnes mediante producción de ácido succínico y ácido lipoteicoico, reduciendo la inflamación y la producción de TNF-alfa e IL-6 inducida por C. acnes en queratinocitos.
Finalmente, los fagos de C. acnes presentan diferencias entre individuos sanos y con acné, sugiriendo que una menor abundancia de fagos puede favorecer el desarrollo de la enfermedad.

Cutibacterium acnes, predominante en áreas sebáceas, está implicado en el desarrollo del acné
Psoriasis
Estudios recientes muestran que la disbiosis de la microbiota cutánea se asocia con la psoriasis, con reducción de Cutibacterium, Burkholderia y Lactobacilli, y aumento de Corynebacterium kroppenstedii, Corynebacterium simulans, Neisseria y Finegoldia en comparación con individuos sanos.
Staphylococcus aureus coloniza hasta el 60 % de las lesiones y su enterotoxina se correlaciona con la gravedad, estimulando la respuesta Th17 y promoviendo la inflamación.
Streptococcus pyogenes también se vincula como factor de riesgo al actuar como superantígeno que activa células T CLA+, aumentando IL-17 y la patogénesis.
Los hongos, como Candida y Malassezia, pueden exacerbar la inflamación.
La disbiosis puede originarse en el intestino, con aumento de Firmicutes y Actinobacteria y disminución de Bacteroides y Akkermansia, perpetuando la inflamación sistémica.
Rosácea
La disbiosis cutánea juega un papel clave en la rosácea al estimular la inmunidad innata. Se observa un aumento de los ácaros Demodex, especialmente D. folliculorum, que segregan compuestos bioactivos y elevan la expresión de TLR2 e IL-8, contribuyendo a la inflamación temprana.
Demodex actúa como vector de bacterias, incluyendo S. epidermidis, Chlamydophila pneumoniae y varias especies de Bacillus, destacando B. oleronius, que induce proliferación de células mononucleares y producción de citocinas proinflamatorias, promoviendo el reclutamiento de neutrófilos y la neoangiogénesis.
La temperatura elevada de la piel afectada puede inducir que S. epidermidis comensal se comporte como patógeno, produciendo factores de virulencia.
Además, Corynebacterium kroppenstedtii y D. folliculorum tienen relación mutualista, y su presencia es necesaria para la supervivencia de los ácaros, mientras que otras bacterias como Roseomonas disminuyen en pacientes con rosácea en comparación con controles sanos.

La disbiosis cutánea juega un papel clave en la rosácea al estimular la inmunidad innata
Productos basados en microbiomas y salud de la piel: enfoques del tratamiento
Los productos basados en microbiomas (MBP) incluyen microorganismos vivos, inactivos, sus componentes o metabolitos que pueden ofrecer beneficios para la salud de la piel o actuar como agentes terapéuticos.
La terminología ha evolucionado desde los probióticos, definidos por la OMS como microorganismos vivos con beneficio para la salud, hasta los Productos Bioterapéuticos Vivos (LBP), que se refieren específicamente a microorganismos vivos con fines terapéuticos, excluyendo postbióticos y fagos. El término MBP se utiliza para englobar todas las formulaciones derivadas del microbioma con potencial terapéutico o preventivo.
La modulación del sistema inmunológico a través de la restauración de la homeostasis microbiana es un enfoque prometedor para enfermedades inflamatorias de la piel. La aplicación de MBP, tanto oral como tópica, ha crecido en la última década, mostrando potencial en la prevención y manejo de patologías como dermatitis atópica, dermatitis seborreica, acné, psoriasis y rosácea, aunque los estudios clínicos aún son limitados.
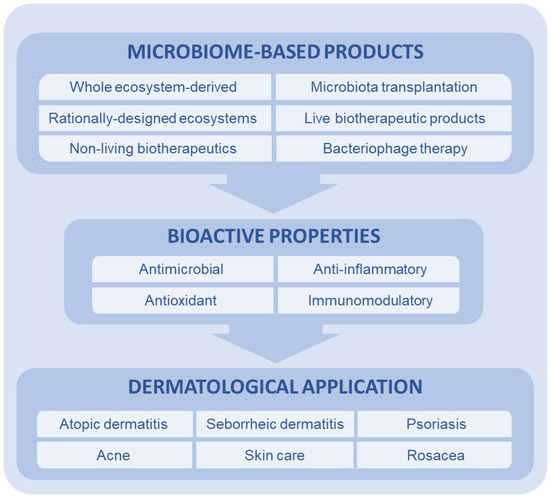
Descripción general de los productos basados en microbioma (MBP) y sus propiedades y aplicaciones bioactivas
MBPs tópicos
Los MBP tópicos buscan restaurar la homeostasis microbiana, mejorar la función de la barrera cutánea y mantener el equilibrio entre huésped y microbiota. Incluyen microorganismos vivos o inactivos, lisatos fermentados y extractos. Se ha investigado más en dermatitis atópica (DA), mostrando efectos como aumento de ceramidas, reducción de S. aureus y mejoría de síntomas.
- Bacterias lácticas (LAB): cepas de Streptococcus, Lactobacillus y Lacticaseibacillus han mostrado restaurar la barrera, reducir inflamación y modular la microbiota cutánea en la DA y DS.
- Roseomonas mucosa: tratamiento tópico con R. mucosa viva disminuyó gravedad de DA y necesidad de esteroides, reduciendo S. aureus.
- Fagos: estudios en modelos animales y pequeños ensayos muestran reducción de S. aureus y mejora de lesiones en DA.
- Acné: lactobacilos vivos y lisatos tópicos reducen C. acnes y mediadores inflamatorios; Bacillus y Enterococcustambién mostraron eficacia. Terapias con fagos dirigidos a C. acnes son prometedoras, seguras y bien toleradas.
- Psoriasis y rosácea: escasamente estudiadas; solo algunos modelos animales sugieren potencial terapéutico de Lactobacillus y fagos.
En general, los MBP tópicos se perciben como seguros y con menos efectos adversos que los tratamientos estándar (corticoides y antibióticos), pero la evidencia clínica aún es limitada
MBPs orales
La microbiota intestinal regula el sistema inmunológico y su disbiosis se asocia con DA, acné, psoriasis y rosácea, lo que abre oportunidades para MBP orales como estrategia terapéutica
- Dermatitis atópica: trasplante de microbiota fecal y cepas probióticas (Bifidobacterium, Lactobacillus, Faecalibacterium, Akkermansia) mejoraron inflamación, barrera epidérmica y marcadores clínicos en modelos animales y ensayos clínicos.
- Acné: MBP orales mostraron efectos antiinflamatorios y antibacterianos en estudios in vitro, modelos animales y ensayos clínicos (L. rhamnosus, Bifidobacterium, Weissella viridescens, Arthrospira).
- Psoriasis y dermatitis seborreica: estudios limitados, algunos modelos animales sugieren beneficio de L. pentosus y L. paracasei.
- Rosácea: evidencia incipiente con combinación de probióticos y tratamiento estándar mostrando mejoría clínica.
Cabe mencionar que hasta el momento no se han aprobado productos terapéuticos tópicos basados en microbioma para enfermedades cutáneas, y la mayoría de formulaciones se usan como productos cosméticos.
Conclusiones
Los productos basados en microbiomas (MBP) constituyen un enfoque terapéutico prometedor para diversas enfermedades inflamatorias de la piel. Su objetivo principal es restaurar la homeostasis microbiana y modular las respuestas inmunitarias, abordando así la fisiopatología subyacente de estas enfermedades crónicas.
Los MBP presentan ventajas significativas al ofrecer un mecanismo multifacético que incluye la modulación del eje intestino-piel, la mejora de la función de la barrera cutánea y la reducción de la inflamación sistémica.
A pesar de su potencial, persisten desafíos importantes. La complejidad del microbioma cutáneo y la variabilidad interindividual dificultan el desarrollo de tratamientos estandarizados. Además, los efectos a largo plazo de la modulación microbiana aún no se conocen completamente. Se requiere investigación adicional para esclarecer los mecanismos de acción de los MBP y realizar ensayos clínicos que evalúen su seguridad y eficacia en formulaciones tópicas.
De cara al futuro, la integración de la medicina personalizada basada en el perfil del microbioma podría optimizar las terapias
Microbiota de la piel
Fuente
Rušanac A, Škibola Z, Matijašić M, et al. Microbiome-based products: therapeutic potential for inflammatory skin diseases. Int J Mol Sci 2025 Jul 14;26(14):6745.









