La creciente comprensión de la fisiopatología de la diabetes ha revelado que muchos pacientes no encajan claramente en la clasificación tradicional de diabetes tipo 1 o tipo 2. El estudio de estas formas “diabetes atípicas” está contribuyendo a identificar nuevos endotipos de la enfermedad
Lugones Editorial©
La frecuencia de la diabetes que no corresponde claramente a diabetes tipo 1 (DM1) ni a diabetes tipo 2 (DM2), actualmente denominada diabetes atípica, probablemente esté subestimada. Su proporción varía entre 5% y 11% según las características étnicas y otras variables de la población estudiada.
A medida que avanza el conocimiento sobre la fisiopatología de la diabetes, se reconoce que algunos pacientes presentan formas de enfermedad que no encajan plenamente en las categorías clásicas. El estudio de estas variantes ha contribuido a ampliar la comprensión de los mecanismos que regulan la secreción de insulina, la sensibilidad a la insulina y la autoinmunidad de los islotes pancreáticos, y ha impulsado el concepto de endotipos fisiopatológicos.
En esta revisión, los autores describen los principales conocimientos clínicos y biológicos derivados del estudio de formas conocidas de diabetes atípica y proponen un marco para identificar a estos pacientes a partir de sus características clínicas, metabólicas y moleculares, así como recursos clínicos y genéticos útiles para su evaluación.
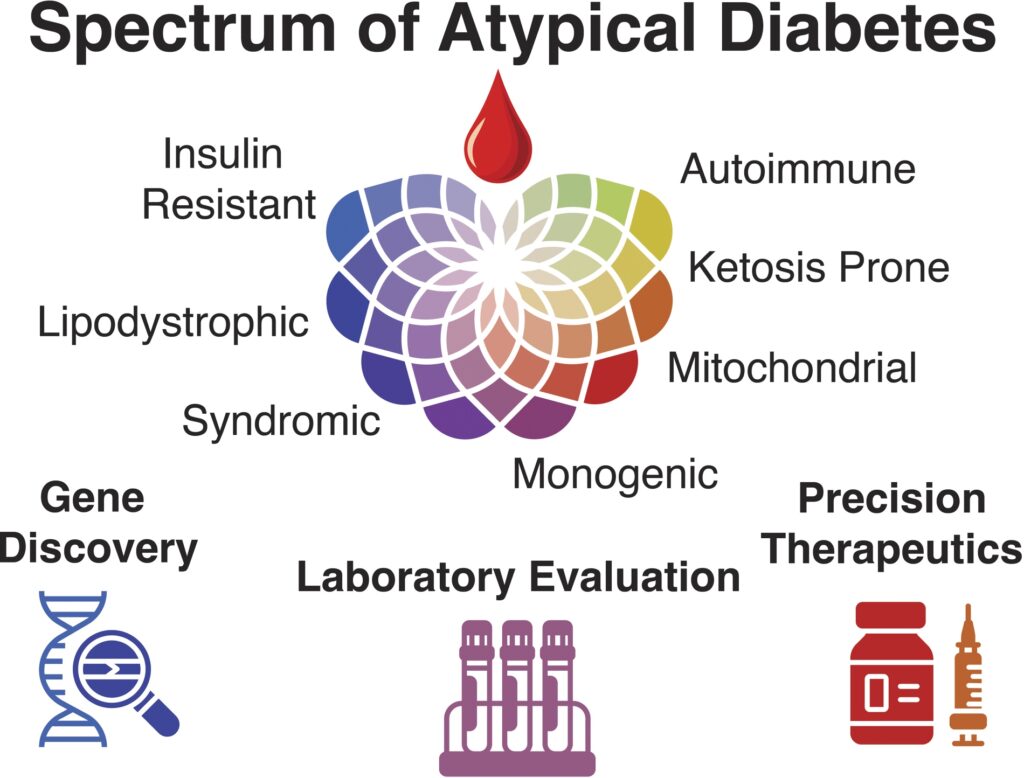
Detectar los distintos endotipos asociados con la diabetes atípica permitirá mejorar la precisión diagnóstica y facilitar decisiones terapéuticas más específicas.
Diabetes atípica
Actualmente se reconoce que la clasificación tradicional de la diabetes en tipo 1 (DM1) y tipo 2 (DM2) es insuficiente para reflejar la diversidad de fenotipos metabólicos y clínicos, así como los distintos mecanismos moleculares y patogénicos que conducen al desarrollo de hiperglucemia. En este contexto surge el concepto de diabetes atípica, que agrupa formas de diabetes que no encajan claramente en las categorías clásicas.
La frecuencia de estas formas probablemente se encuentra subestimada y podría representar entre 5% y 11% de los casos, dependiendo de las características de la población estudiada. Se sospecha diabetes atípica en pacientes que no cumplen plenamente los criterios clínicos de DM1, DM2 o diabetes secundaria.
El estudio de estas entidades ha permitido introducir el concepto de endotipos de diabetes, en el que los pacientes se agrupan según mecanismos clínicos, moleculares o genéticos compartidos. Este enfoque busca mejorar la comprensión de la heterogeneidad de la enfermedad y proporcionar un marco para evaluar a pacientes con presentaciones clínicas no típicas.
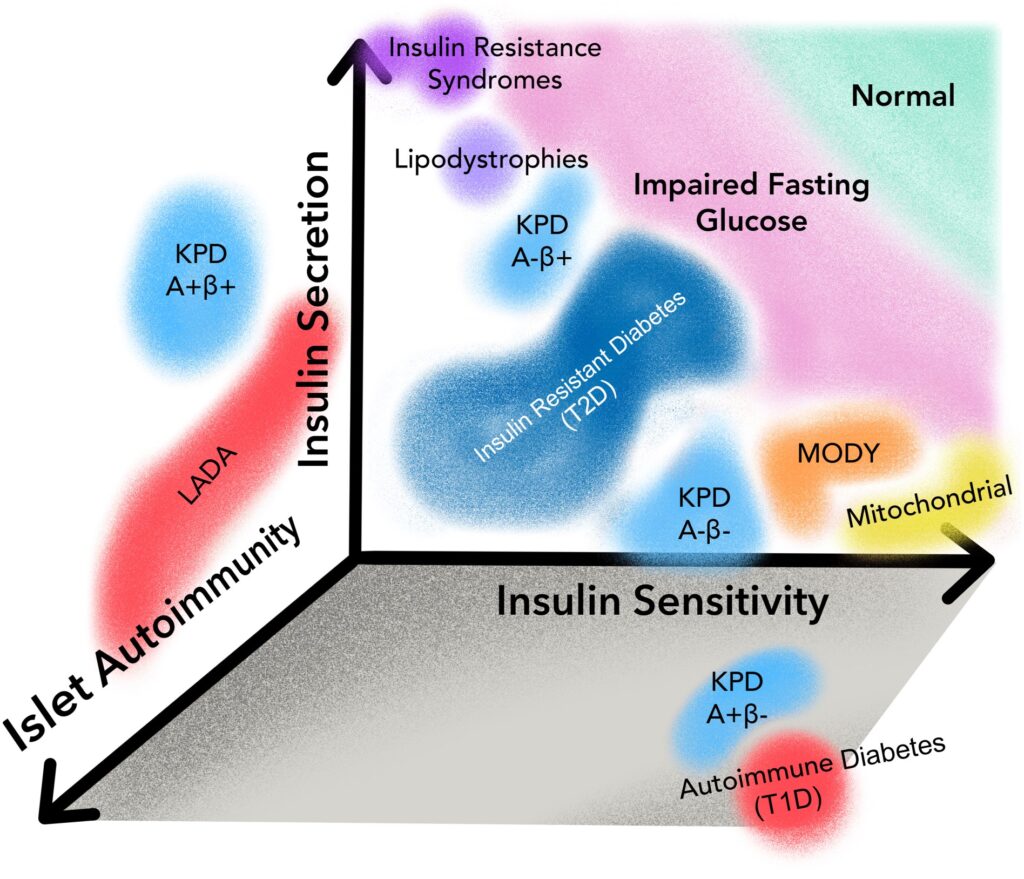
Conceptualización de subtipos de diabetes dentro de tres ejes: sensibilidad a la insulina, secreción de insulina y autoinmunidad de islotes
Diabetes monogénica
La diabetes monogénica corresponde a formas no sindrómicas de DM causadas por variantes patogénicas en un único gen con herencia mendeliana. Las presentaciones más conocidas son la DM de inicio en la madurez de los jóvenes (MODY) y la DM neonatal, muchas veces vinculadas con alteraciones en genes clave para el desarrollo o la función de la célula β.
Un antecedente familiar fuerte, con patrón autosómico dominante y múltiples generaciones afectadas, suele ser una característica distintiva, aunque con frecuencia estos pacientes son diagnosticados erróneamente como DM1 o DM2.
Ejemplos de diabetes monogénica
- GCK-MODY (MODY 2)
Es la forma más frecuente de MODY y se debe a variantes en el gen GCK, que codifica la glucoquinasa, enzima que actúa como sensor de glucosa en la célula β. Se caracteriza por hiperglucemia leve y estable, generalmente sin factores de riesgo metabólicos ni aumento del riesgo de complicaciones microvasculares, por lo que habitualmente no requiere tratamiento farmacológico.
- HNF1A-MODY (MODY 3)
Es la segunda forma más común y resulta de variantes en el gen HNF1A, un factor de transcripción importante para la función de la célula β. Suele manifestarse en la adolescencia o en adultos jóvenes con deficiencia progresiva de insulina y riesgo de complicaciones microvasculares si no se trata adecuadamente. Muchos pacientes responden bien a sulfonilureas, especialmente cuando el diagnóstico se realiza precozmente.
- Diabetes neonatal
Se diagnostica habitualmente antes de los 6 meses de vida y con frecuencia se asocia con mutaciones en los genes KCNJ11 o ABCC8, que codifican subunidades del canal KATP. Su evolución es variable, desde formas transitorias hasta diabetes permanente, y en casos raros puede asociarse con retraso del desarrollo y epilepsia.
- Formas oligogénicas
Además de las formas monogénicas clásicas, se reconocen modelos digénicos u oligogénicos, en los que variantes en dos o más genes contribuyen al desarrollo de diabetes. Estos hallazgos, impulsados por los avances en secuenciación genética, están ampliando la comprensión de la heterogeneidad genética de la diabetes atípica y favoreciendo el desarrollo de enfoques de diabetes de precisión.

La diabetes neonatal se diagnostica habitualmente antes de los 6 meses de vida y con frecuencia se asocia con mutaciones en los genes KCNJ11 o ABCC8, que codifican subunidades del canal KATP.
Diabetes sindrómica
Las formas sindrómicas de DM se caracterizan por la presencia de hiperglucemia asociada a otras manifestaciones clínicas, resultado de un mismo defecto molecular. Estas entidades suelen involucrar múltiples órganos, ya que los genes implicados participan no solo en la función de la célula β sino también en procesos biológicos de otros tejidos.
Aunque un antecedente familiar puede sugerir una etiología genética, algunas formas se deben a mutaciones de novoy pueden presentarse como casos aparentemente esporádicos. Las manifestaciones extrapancreáticas pueden incluir compromiso neurológico, endocrino, esquelético, gastrointestinal o inmunológico, dependiendo del gen afectado.
En la diabetes sindrómica, las manifestaciones extrapancreáticas pueden incluir compromiso neurológico, endocrino, esquelético, gastrointestinal o inmunológico, dependiendo del gen afectado
- Síndrome de Wolfram
El síndrome de Wolfram es un ejemplo clásico de DM sindrómica. Se asocia con variantes bialélicas en WFS1 o CISD2 y se hereda de forma autosómica recesiva.
Los pacientes suelen presentar antes de los 16 años una diabetes con deficiencia de insulina y anticuerpos negativos, seguida de atrofia óptica. Con el tiempo pueden aparecer otras manifestaciones, como hipoacusia neurosensorial, diabetes insípida, anomalías urinarias, neurodegeneración progresiva y trastornos psiquiátricos.
A nivel fisiopatológico, la alteración de la proteína wolframina provoca estrés del retículo endoplásmico, lo que afecta la síntesis normal de insulina en la célula β.

El síndrome de Wolfram es un ejemplo clásico de diabetes sindrómica. Se asocia con variantes bialélicas en WFS1 o CISD2 y se hereda de forma autosómica recesiva
Diabetes mitocondrial
La diabetes mitocondrial se debe a alteraciones en la función mitocondrial y muestra gran heterogeneidad clínica. Puede heredarse por línea materna cuando las variantes están en el ADN mitocondrial o como autosómica recesiva si afectan genes nucleares. Un ejemplo es la variante m.3243A>G, asociada al síndrome de diabetes y sordera de herencia materna (MIDD). Su reconocimiento es importante porque la metformina está contraindicada por el riesgo de acidosis láctica.
Formas lipodistróficas de diabetes
Las lipodistrofias se caracterizan por pérdida de tejido adiposo generalizada o parcial, lo que provoca resistencia severa a la insulina, hipertrigliceridemia y esteatosis hepática. Estas entidades han contribuido a comprender el papel endocrino del tejido adiposo y de adipocinas como leptina y adiponectina en el metabolismo.
- Lipodistrofia generalizada congénita
Se caracteriza por ausencia casi completa de tejido adiposo desde la infancia y resistencia extrema a la insulina. Los pacientes suelen requerir dosis muy altas de insulina; la metreleptina es una opción terapéutica en algunos casos.
- Lipodistrofia familiar parcial
Produce pérdida de grasa en extremidades y caderas con acumulación en otras regiones, y suele manifestarse en la adolescencia. Se asocia con variantes en genes como LMNA o PPARG y con frecuencia requiere tratamiento intensivo de hiperglucemia y dislipidemia.

Las lipodistrofias se caracterizan por pérdida de tejido adiposo generalizada o parcial, lo que puede provocar resistencia severa a la insulina, hipertrigliceridemia y esteatosis hepática
- Síndromes progeroides
Los síndromes progeroides simulan envejecimiento acelerado y pueden asociarse con lipodistrofia, resistencia a la insulina e hipertrigliceridemia. La diabetes suele ser leve o moderada.
- Lipodistrofia generalizada adquirida
La lipodistrofia generalizada adquirida se caracteriza por pérdida progresiva de grasa corporal, a menudo asociada con enfermedades autoinmunes. El tratamiento incluye terapias habituales para la resistencia a la insulina y, en algunos casos, metreleptina.
Diabetes autoinmune latente (LADA)
La LADA se define por la presencia de autoanticuerpos de islote en adultos que inicialmente no requieren insulina. Con frecuencia se clasifica como DM2, aunque comparte características fisiopatológicas con DM1 y DM2. Su prevalencia entre pacientes diagnosticados como DM2 se estima entre 5% y 13%.
Diabetes propensa a la cetosis
La diabetes propensa a la cetosis (KPD) se presenta con cetoacidosis al diagnóstico sin autoanticuerpos típicos de DM1. Algunos pacientes recuperan función de células β y pueden suspender la insulina tras el episodio inicial.
Diabetes fulminante
La diabetes fulminante se caracteriza por inicio muy brusco con cetoacidosis y HbA1c normal o casi normal al diagnóstico. Aunque suele considerarse un subtipo de DM1, generalmente no presenta autoanticuerpos y la destrucción de células β ocurre en pocas semanas.
Síndromes graves de resistencia a la insulina
Los síndromes graves de resistencia a la insulina se caracterizan por hiperinsulinemia marcada y manifestaciones como acantosis nigricans, hirsutismo, síndrome de ovario poliquístico y alteraciones menstruales, generalmente sin pérdida de tejido adiposo. Algunos se deben a variantes en el gen del receptor de insulina (INSR), como el síndrome de Donohue o el de Rabson-Mendenhall. Estos pacientes suelen requerir altas dosis de insulina, y en algunos casos pueden beneficiarse de terapias dirigidas como sensibilizadores de insulina o IGF-1 recombinante.
Diabetes secundaria a enfermedad pancreática
La diabetes pancreatogénica (tipo 3c) se asocia con enfermedades del páncreas exocrino, como fibrosis quística, hemocromatosis, pancreatitis crónica, cáncer de páncreas o pancreatectomía. Representa un grupo heterogéneo en el que los mecanismos que conducen a la hiperglucemia no siempre están completamente definidos.

La diabetes pancreatogénica (tipo 3c) se asocia con enfermedades del páncreas exocrino, como fibrosis quística, hemocromatosis, pancreatitis crónica, cáncer de páncreas o pancreatectomía
Enfoque del paciente
La sospecha de diabetes atípica surge cuando la presentación clínica no encaja claramente con DM1 o DM2. Un antecedente familiar detallado puede aportar pistas, especialmente en formas genéticas como la diabetes monogénica.
También pueden orientar el diagnóstico manifestaciones extrapancreáticas (por ejemplo, sordera en diabetes mitocondrial o características sindrómicas), así como patrones clínicos inusuales, como cetoacidosis inicial con posterior remisión de la insulina en la diabetes propensa a la cetosis.
El examen físico puede revelar signos de resistencia a la insulina (acantosis nigricans), alteraciones del tejido adiposo sugestivas de lipodistrofia u otros hallazgos sindrómicos.
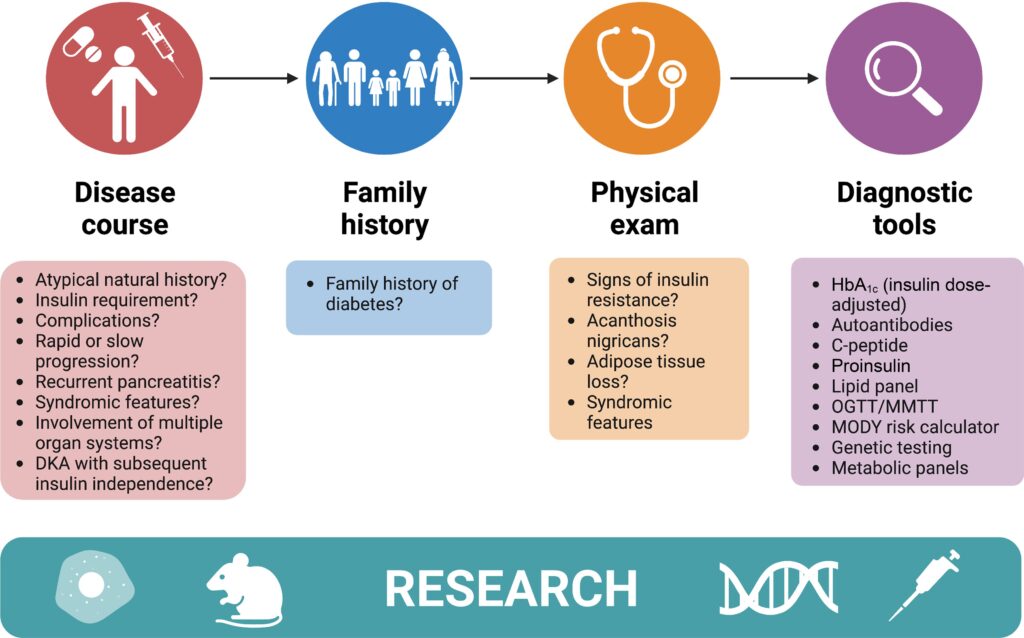
Acercamiento al paciente con diabetes atípica
- Pruebas clínicas útiles
La evaluación de la diabetes atípica incluye pruebas que permitan caracterizar autoinmunidad, función de células β, resistencia a la insulina y causas genéticas.
. Autoanticuerpos de islote (GAD65, IA-2, insulina, ZnT8) ayudan a identificar diabetes autoinmune.
. Péptido C o insulina sérica permiten estimar la reserva funcional de células β.
. Pruebas dinámicas como OGTT o test de comida mixta pueden evaluar secreción de insulina y resistencia a la insulina.
En algunos casos, calculadoras clínicas y pruebas genéticas pueden ayudar a identificar diabetes monogénica.
- Pruebas genéticas
Las pruebas genéticas son fundamentales para confirmar algunas formas de diabetes atípica, especialmente diabetes monogénica. Las guías actuales recomiendan considerarlas cuando las características clínicas sugieren una etiología genética.
Los métodos de secuenciación genética de nueva generación han ampliado la capacidad diagnóstica, aunque la interpretación de los resultados puede ser compleja y requiere asesoramiento adecuado.

Las pruebas genéticas son fundamentales para confirmar algunas formas de diabetes atípica, especialmente diabetes monogénica
Diabetes atípica y medicina de precisión
Los enfoques actuales de medicina de precisión en diabetes atípica buscan identificar subtipos definidos por mecanismos clínicos, genéticos y moleculares, con el objetivo de orientar estrategias terapéuticas individualizadas.
El modelo ideal plantea una clasificación endotípica basada en datos genómicos, transcriptómicos y metabolómicos, aunque su aplicación clínica aún es limitada.
Iniciativas de investigación como la Rare and Atypical Diabetes Network (RADIANT) buscan caracterizar las distintas formas de diabetes atípica, sus bases fisiopatológicas y sus manifestaciones clínicas. Este tipo de proyectos permitirá, en el futuro, integrar herramientas ómicas en el diagnóstico y tratamiento, avanzando hacia una clasificación más precisa y una atención personalizada en diabetes.
Conclusiones
La diabetes atípica comprende un conjunto heterogéneo de formas de diabetes que no encajan claramente en las categorías tradicionales de DM1 o DM2. Su reconocimiento requiere considerar características clínicas, antecedentes familiares y estudios complementarios que orienten hacia etiologías específicas.
El avance en la caracterización de endotipos y en herramientas genómicas y multiómicas podría mejorar la clasificación de estos pacientes y contribuir, en el futuro, al desarrollo de estrategias de diagnóstico y tratamiento más individualizadas.

La diabetes puede interpretarse a través de endotipos fisiopatológicos, definidos por tres ejes principales: secreción de insulina, sensibilidad a la insulina y autoinmunidad de los islotes pancreáticos
Diabetes atípica: más allá de la clasificación en tipo 1 y tipo 2
Fuente
Stone SI, Balasubramanyam A, Posey JE. Atypical diabetes: What have we learned and what does the future hold? Diabetes Care 2024;47(5).