Avances terapéuticos y direcciones futuras en relación al tratamiento de la epidermólisis ampollosa, también llamada piel de cristal
Lugones Editorial©
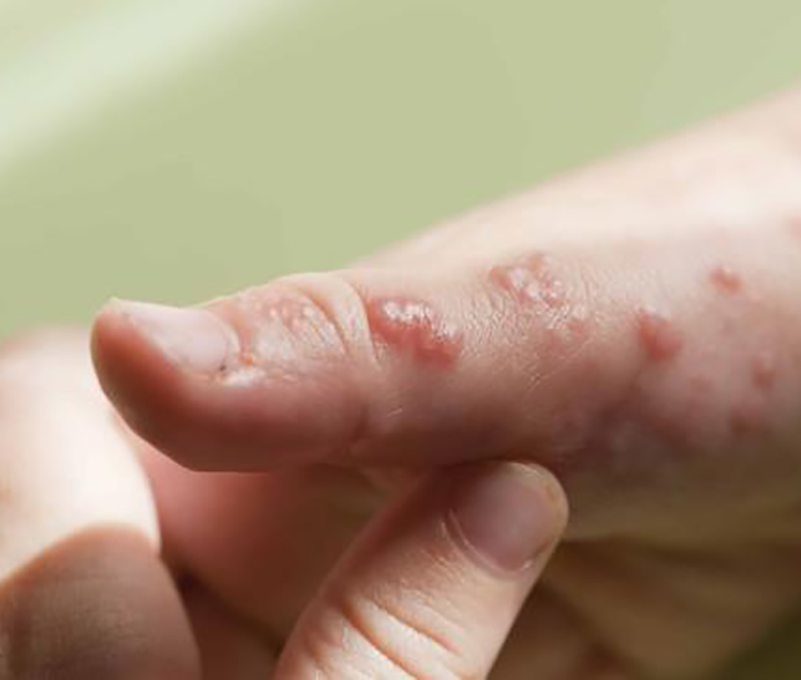
La epidermólisis ampollosa (EB), también llamada “piel de cristal”, comprende trastornos genéticos raros caracterizados por ampollas en la piel y la membrana mucosa inducidas por un trauma mecánico. En los últimos 30 años se han investigado varias vías de tratamiento con nuevos enfoques terapéuticos.
El manejo de la epidermólisis ampollosa es multidisciplinario, y se centra en el apoyo a la cicatrización de las heridas. Luego de años de investigación, los nuevos enfoques terapéuticos se enfrentan a desafíos:
- La terapia génica y la terapia de proteínas luchan con la eficacia.
- Las terapias regenerativas basadas en células muestran efectos limitados.
- La reutilización de medicamentos para atacar varios mecanismos patógenos ha llamado la atención, al igual que la terapia génica in vivo con medicamentos para EB distrófica y de unión que fueron aprobados recientemente por la FDA y la EMA.
Los autores del presente artículo presentan el desarrollo de los nuevos enfoques terapéuticos, basados en la investigación sistemática de la literatura que cubre los últimos 5 años en relación a la piel de cristal.
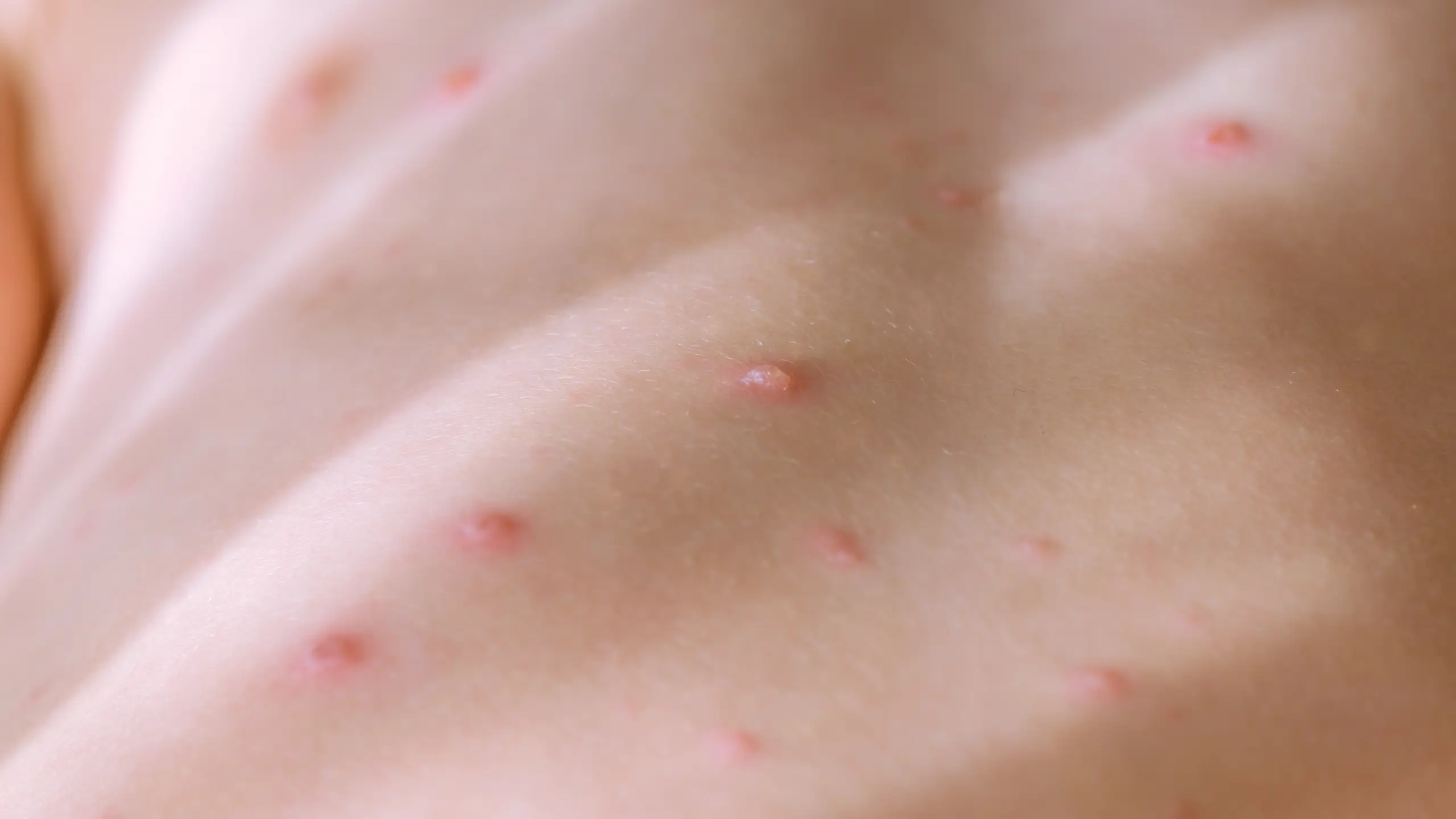
La epidermólisis bullosa (EB), o piel de cristal, se subdivide en cuatro tipos principales: EB simplex (EBS), EB de la unión (JEB), EB distrófica (DEB) y EB Kindler
Terapia de reemplazo genético
- Reemplazo genético in vivo. Krystal Biotech ha desarrollado una terapia génica tópica conocida como beremagene geperpavec (B-VEC) que utiliza un virus de herpes simple de replicación no integrada-defectuosa-1 (HSV-1) que contiene dos copias del genCOL7A1. Este enfoque facilita la expresión de polipéptidos proα1 (VII) en la piel, permitiendo su integración en moléculas triméricas C7 y posterior ensamblaje en fibrillas de anclaje funcional. B-VEC se convirtió en el primer tratamiento de terapia génica accesible para personas con EB. Actualmente se está llevando a cabo un estudio observacional continuo con seguimiento a largo plazo de todos los pacientes tratados con un vector HSV-1 y tiene una fecha de finalización anticipada en 2028 (NCT04917887).
- Terapia génica ex vivo. El trasplante de queratinocitos transgénicos en el 80% de la superficie corporal fue innovador en 2017. Cinco años de seguimiento demostraron que las células madre reparadas genéticamente sobrevivieron y continuaron regenerando una epidermis casi normal
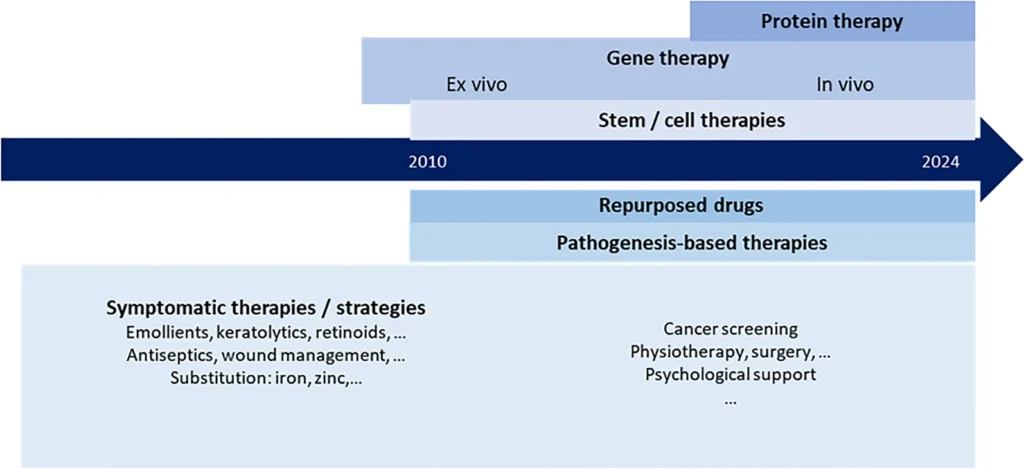
Cadena patogénica en la EB grave, en particular la EBD. La fragilidad cutánea y las heridas son las manifestaciones iniciales de la EB y provocan complicaciones cutáneas y sistémicas. Por lo tanto, las terapias correctivas dirigidas a la adición de colágeno tipo VII a la piel constituyen un enfoque eficaz.
Terapia génica natural o mosaicismo revertiente
El mosaicismo revertiente, o “terapia génica natural”, se muestra prometedor para la terapia celular en la EB, donde ciertas células cutáneas revierten espontáneamente mutaciones, dando lugar a áreas de piel normal. Los mecanismos incluyen recombinaciones mitóticas, retromutaciones y mutaciones de segundo sitio.
Los desafíos en el cultivo a largo plazo se deben a la disminución de células madre, pero el injerto en sacabocados de piel revertiente sobre lesiones ha dado lugar a una reepitelización limitada. La expansión puede lograrse generando células madre pluripotentes inducidas (iPSC) a partir de queratinocitos revertientes y diferenciándolas en queratinocitos corregidos.
Estas iPSC revertientes ofrecen el potencial para la terapia celular en la EB, aunque su naturaleza personalizada limita su amplia aplicación clínica.
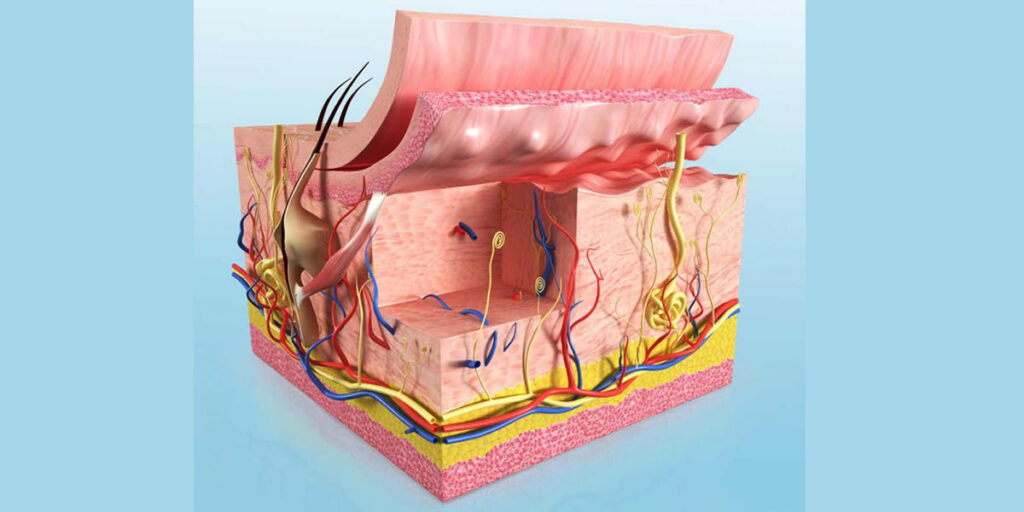
Las terapias correctivas dirigidas son la forma definitiva de tratar la epidermólisis bullosa
Edición genética
Las técnicas de edición genética, como las repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas (CRISPR/Cas9), ofrecen el potencial para tratar la EB mediante la corrección de mutaciones y la mejora de la eficacia de la corrección genética en células derivadas de pacientes, lo que permite el desarrollo de injertos de piel funcionales que sintetizan colágeno.
Los desafíos incluyen la necesidad de una gran cantidad de células cultivadas, que se aborda mediante soluciones como las iPSC. Las nucleasas efectoras similares a activadores de la transcripción (TALEN) y CRISPR/Cas9 se han utilizado con éxito en la edición genética para la EB para generar una mayor estabilidad en los equivalentes de piel (SE) editados genéticamente.
Las técnicas de edición de bases y la edición principal son prometedoras en la corrección de mutaciones puntuales. Sin embargo, persisten desafíos en la traducción clínica, incluyendo los efectos fuera del objetivo y la eficacia en la piel no lesionada.
Salto de exones y otras terapias basadas en ARN
La omisión de exón utiliza oligonucleótidos antisentido (ASO) para alterar el empalme del ARN premensajero (ARNm), eliminando así la mutación responsable de la enfermedad. Inicialmente desarrollada para la distrofia muscular de Duchenne (DMD), la omisión de exón mediada por antisentido ha progresado hasta ensayos clínicos dirigidos a exones con mutaciones recurrentes en el gen de la distrofina.
Si bien la administración directa de ASO a las células de la herida es factible, también se están realizando esfuerzos para mejorar la administración en la piel intacta mediante liposomas catiónicos.
| Terapia génica | Reemplazo de genes ex vivo |
| Reemplazo de genes in vivo | |
| Edición de genes ex vivo | |
| Uso de mosaicismos reverberantes | |
| Basadas en ARN | |
| Terapia basada en células | Queratinocitos y fibroblastos |
| Membrana amniótica | |
| Injertos de piel bioingenierizada | |
| Células madre estromales/mesenquimáticas | |
| Terapia de reemplazo de la proteína faltante | |
| Terapia de lectura completa del codón de terminación prematura | |
| Misceláneas | Diacereína |
| Apremilast | |
| Losartán | |
| Biológicos | |
| HMBG-1 | |
| Timosina β4 | |
| Oleogel S-100 |
Clasificación de los nuevos tratamientos contra la epidermólisis ampollar
Terapia de proteínas
El tratamiento con proteínas recombinantes es prometedor para las formas recesivas de EB caracterizadas por mutaciones de pérdida de función, como C7 en la epidermólisis bullosa distrófica recesiva (RDEB) y laminina-332 en la EB de la unión (JEB). Estudios en ratones demostraron que la inyección de C7 recombinante en la piel indujo la formación de fibrillas de anclaje sin una unión significativa de anticuerpos.
La administración intravenosa de C7 recombinante se dirigió a la piel y promovió la formación de fibrillas de anclaje, con una unión mínima de anticuerpos a la membrana basal cutánea.
En este sentido, la terapia con C7 recombinante muestra potencial para complementar las terapias locales, mejorando la función inmunitaria innata y reduciendo la infección en las heridas causadas por EBDR, lo que potencia la eficacia de otros tratamientos cutáneos localizados.

Las técnicas de edición de bases y la edición principal son prometedoras en la corrección de mutaciones puntuales
Terapias basadas en células
La terapia celular abarca una gama de tratamientos que involucran queratinocitos primarios, fibroblastos, células hematopoyéticas y células madre mesenquimales/estromales.
- Fibroblastos. Múltiples ensayos clínicos en humanos han investigado la eficacia de las inyecciones intradérmicas de fibroblastos alogénicos en heridas crónicas por EBDR. Los resultados han mostrado resultados variables, con una mejora en la cicatrización de entre el 30 y el 80%.
- Trasplante de médula ósea. En modelos murinos de RDEB, las células madre hematopoyéticas se diferenciaron en células epidérmicas, generando C7 y prolongando la longevidad. El injerto epidérmico mediante un dispositivo automatizado mínimamente invasivo (CELLUTOME) para obtener microinjertos epidérmicos del mismo donante tras un trasplante alogénico de células hematopoyéticas mostró una adhesión prolongada, con una duración de hasta 3 años sin rechazo. Las células de la médula ósea ayudan a la reparación de la piel y abordan la deficiencia de C7 en modelos murinos con EBDR.
- Células madre mesenquimales. Las células madre mesenquimales (MSC), con capacidad de autorrenovación y diferenciación, ofrecen beneficios potenciales en la terapia con células DEB gracias a sus propiedades inmunomoduladoras y antiinflamatorias. Las MSC se han administrado por vía intradérmica o intravenosa a pacientes con RDEB. La inyección intradérmica ofrece una administración localizada, lo que potencialmente mejora la interacción con las células huésped, mientras que la infusión intravenosa permite un impacto sistémico.
- Terapia de injerto de piel mediante ingeniería tisular. Se está llevando a cabo un estudio piloto para evaluar un sustituto temporal de la piel para la cicatrización de heridas en pacientes con EBDR (NCT05944250). Se utiliza un dispositivo portátil, el primero de su tipo, diseñado para administrar un apósito de matriz nanofibrosa electrohilada, no invasivo y no terapéutico, a las heridas, lo que facilita el proceso de cicatrización.
Terapias basadas en la patogénesis y fármacos reutilizados
Estos enfoques pueden incluir la reutilización de fármacos existentes o la creación de nuevas terapias, con el objetivo de aliviar la gravedad de la enfermedad y mejorar el bienestar del paciente.
Medicamentos que mejoran la cicatrización de heridas
- Grupo de alta movilidad Box-1 (HMGB1). Es una proteína nuclear que, al liberarse de las células, puede actuar como un mediador de la inflamación y un desencadenante de la respuesta inmunitaria. Los modelos animales han demostrado que la administración sistémica del fragmento HMGB1 es beneficiosa, preservando la función cardíaca en hámsteres deficientes en delta-sarcoglicano y mejorando las manifestaciones en ratones modelo DEB.
- Oleogel-S10. Oleogel-S10 demostró acelerar la cicatrización de las heridas al modular la inflamación, promover la migración de queratinocitos y ejercer efectos antimicrobianos. Previamente utilizados en quemaduras y heridas de injertos de piel de espesor parcial, estos extractos aceleran el cierre de la herida.

En cuanto a la terapia celular, se ha demostrado que los efectos a largo plazo son limitados y que no se ha logrado la aplicación clínica
- Calcipotriol. En un ensayo aleatorizado y controlado con placebo en el que participaron seis pacientes con RDEB, las lesiones tratadas con calcipotriol mostraron una reducción significativa del área herida (88%) en comparación con el placebo (66%). Además, los niveles de picazón disminuyeron significativamente entre 2 y 4 semanas después del inicio del tratamiento. Si bien los resultados son prometedores, actualmente no existen recomendaciones ni formulaciones específicas de calcipotriol para su uso en RDEB.
- Medicamentos antiinflamatorios. El análisis computacional identificó al metotrexato como un candidato prometedor para revertir estos patrones de expresión génica, lo que sugiere su potencial para aliviar la inflamación sistémica y reducir el prurito en la RDEB. Además, el aumento de la expresión de IL-17A observado en pacientes con DEB sugiere que las moléculas pequeñas y los productos biológicos dirigidos a IL-17A, que se utilizan comúnmente en el tratamiento de la psoriasis, también pueden beneficiar a las personas con DEB.
- Terapia antifibrótica. Losartán, un medicamento antihipertensivo, puede atenuar la señalización de TGF-β. Su eficacia se evaluó en un modelo de ratón hipomórfico col7a1, donde retrasó la cicatrización de la pata y la fusión de los dedos, lo que indica un potencial para la terapia RDEB humana. Otro enfoque para reducir la actividad de TGF-β en la piel implica aumentar la expresión de decorina, un proteoglicano estromal que inhibe a TGF-β al unirse a su proteína central, impidiendo su interacción con los receptores. La administración intraperitoneal de decorina fusionada con el péptido de localización cutánea disminuyó notablemente la expresión génica fibrótica y mitigó la fibrosis en la piel de ratones con EBDR.
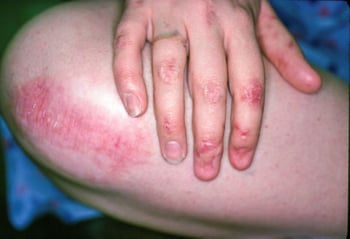
El tratamiento a través de la reutilización de medicamentos (reposicionamiento) está ganando atención
- Terapias antipruriginosas. Dupilumab, un anticuerpo monoclonal dirigido al receptor IL-4 para reducir la actividad de las citocinas IL-4 e IL-13, se ha investigado para el prurito de EB. Varios informes anecdóticos sugieren resultados prometedores con dupilumab, con reducciones rápidas en la gravedad del prurito y la inflamación de la piel observadas en pacientes con EB pruriginosa, pero también en aquellos con otros tipos de EB. Asimismo, serlopitant, un antagonista del receptor de neuroquinina-1 que altera la señalización de la sustancia P, se presenta prometedor como posible tratamiento para el prurito.
- Medicamentos reutilizados para EBS. En este grupo se incluyen a la diacereína que se descubrió que era beneficiosa para estabilizar los filamentos de queratina y disminuir las ampollas en la piel; la timosina β4, un polipéptido natural con diversas propiedades cicatrizantes, como propiedades antiinflamatorias, antifibróticas, proangiogénicas y de reclutamiento de células madre, que se ha estudiado por su potencial para tratar la EB; el apremilast, una molécula anti-Th17, que produjo una mejora significativa en el estado de la piel de pacientes con epidermólisis ampollosa simple generalizada grave (EBS-gen sev); y los inhibidores de mTOR y los inhibidores de la fosfatidilinositol 3-quinasa que demostraron resultados prometedores en el tratamiento de la queratodermia plantar dolorosa resultante de la formación crónica de ampollas en pacientes con EBS.
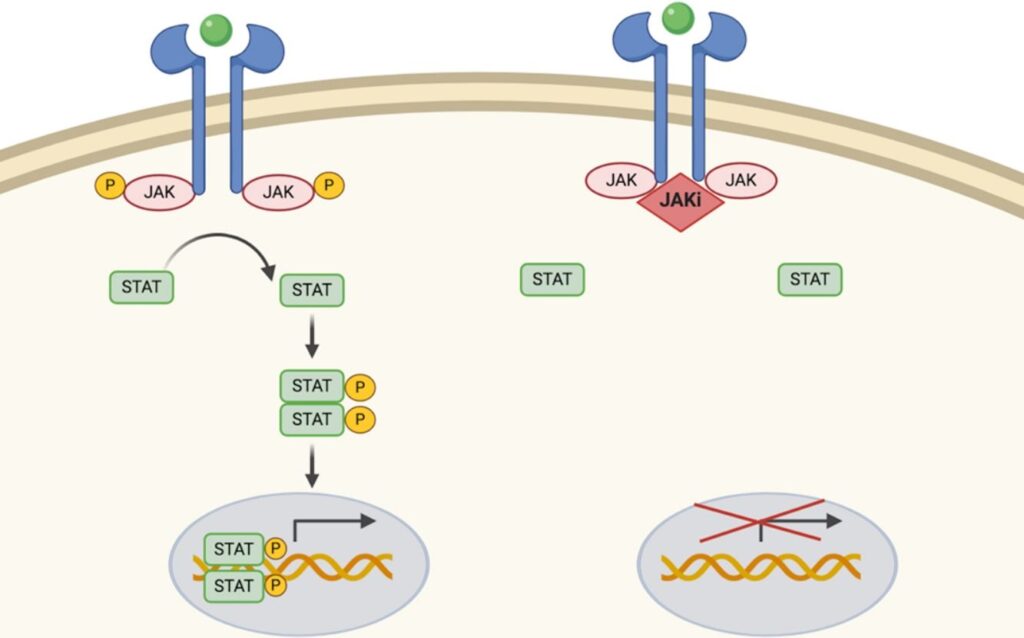
Los inhibidores de IL-4/13 y los inhibidores de JAK, que se utilizan para tratar la dermatitis atópica, son prometedores para tratar el prurito en la EB
Conclusiones
Los defectos genéticos en la EB grave presentan una alta penetrancia y expresividad, y un fuerte impacto en la homeostasis cutánea. Las terapias correctivas dirigidas y la medicina regenerativa, basadas en la reposición de genes, proteínas o células deficientes, ofrecen los únicos tratamientos eficaces, pero siguen siendo complejos y costosos.
Por lo tanto, es necesario centrar los esfuerzos en la implementación de los avances actuales, como la terapia génica in vivo y ex vivo, en la atención clínica de los pacientes. Las terapias complementarias que utilizan fármacos reutilizados menos costosos pueden ayudar a aliviar la gravedad de la enfermedad, en particular en los subtipos menos graves de EB, y mejorar la calidad de vida de las personas afectadas. Estas terapias podrían complementar las estrategias dirigidas a los procesos patológicos subyacentes de la fragilidad de la piel y las mucosas.
Demostrar la eficacia de estas medidas y diseñar ensayos clínicos con criterios de valoración y número de participantes adecuados plantea numerosos desafíos. Sin embargo, los pacientes con EB y sus familias esperan con entusiasmo tratamientos eficaces en un futuro próximo.

Es necesario centrar los esfuerzos en la implementación de los avances actuales, como la terapia génica in vivo y ex vivo, en la atención clínica de los pacientes
Puntos clave
- Las terapias correctivas dirigidas son la forma definitiva de tratar la epidermólisis bullosa (EB).
- La terapia génica in vivo está entrando en la etapa de aplicación clínica. Beremagene geperpavec (B-VEC) ha sido aprobado por la FDA y se ha convertido en la primera terapia génica disponible para pacientes con EB distrófica. Esto puede considerarse un avance significativo.
- El tratamiento a través de la reutilización de medicamentos (reposicionamiento) está ganando atención. Se está considerando la aplicación de medicamentos existentes para atacar mecanismos patógenos como la cicatrización de heridas, la inflamación, el prurito y la fibrosis. Este enfoque se considera relativamente barato y altamente factible.
- Se señala que los inhibidores de IL-4/13 y los inhibidores de JAK, que se utilizan para tratar la dermatitis atópica, son prometedores para tratar el prurito en la EB. Pueden proporcionar nuevas opciones para controlar el prurito y las lesiones cutáneas en la EB.
- En cuanto a la terapia celular, se ha demostrado que los efectos a largo plazo son limitados y que no se ha logrado la aplicación clínica. Los desafíos siguen existiendo en los enfoques de la medicina regenerativa.
- Están surgiendo nuevos conceptos de tratamiento, como la edición genética y la terapia con ARN, pero todavía se encuentran en la etapa preclínica. Se mencionan como posibilidades futuras.
Piel de cristal: tratamientos
Fuente
Danescu S, Negrutiu M, Has C. Treatment of epidermolysis bullosa and future directions: a review. Dermatol Ther (Heidelb) 2024 Aug;14(8):2059-2075.