Artículo que propone un marco conceptual para orientar la investigación y el desarrollo de la nueva era de la dermatología, con énfasis en cuatro desafíos: precisión, traducción, modalidad y curación
Lugones Editorial©
El artículo “Grand challenges in dermatologic drug discovery: four priorities to transform skin disease treatment” identifica cuatro grandes desafíos que pueden redefinir la nueva era de la dermatología:
- Precisión terapéutica, con biomarcadores predictivos para seleccionar tratamientos personalizados.
- Traducción más sólida de descubrimientos preclínicos a los ensayos en humanos.
- Modalidades terapéuticas innovadoras, como terapias génicas, degradadores de proteínas, delivery dirigido, etc.
- Curación real de enfermedades cutáneas, más allá de la simple supresión de síntomas.
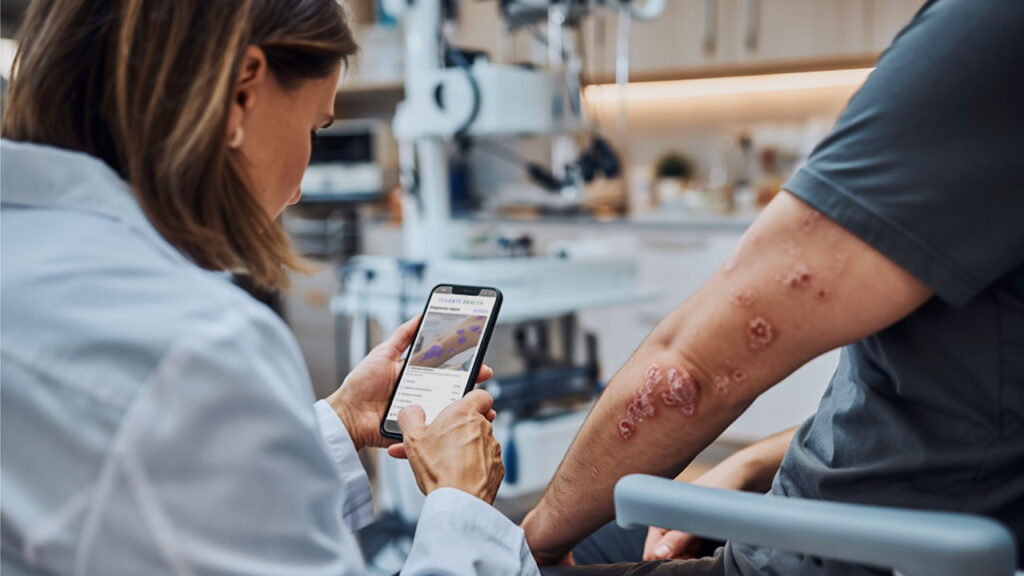
Los avances en dermatología son notables, pero incluso las mejores terapias actuales no ofrecen respuestas duraderas, universales ni curativas
En la última década, la dermatología se ha beneficiado de terapias dirigidas que antes eran inimaginables. Los biológicos y las pequeñas moléculas inhibidoras de JAK desempeñan hoy un papel central en múltiples enfermedades, especialmente en psoriasis y dermatitis atópica, mientras que plataformas emergentes, como los anticuerpos multiespecíficos, están bajo evaluación activa.
La inhibición de la vía Janus quinasa–transductor de señal y activador de la transcripción (JAK-STAT) ha ampliado las opciones terapéuticas en enfermedades como la dermatitis atópica, la alopecia areata y el vitiligo, y ha modificado la forma en que se definen los puntos finales de eficacia y los objetivos de tratamiento en los ensayos clínicos y en la práctica.
Sin embargo, este progreso no ha eliminado el problema central que sigue definiendo gran parte de la práctica dermatológica: muchos pacientes no responden a las terapias disponibles o pierden la respuesta con el tiempo, de modo que incluso los tratamientos más avanzados rara vez logran una remisión duradera o una curación.
Primer gran desafío: la precisión
La autora sostiene que la dermatología de precisión comienza al reconocer que enfermedades como la dermatitis atópica y la psoriasis no son entidades únicas, sino síndromes heterogéneos formados por fenotipos que comparten manifestaciones clínicas, pero difieren en sus mecanismos moleculares, comorbilidades, evolución y respuesta al tratamiento.
Esta heterogeneidad explica por qué, a pesar del impacto de los biológicos, una proporción sustancial de pacientes no alcanza respuestas clínicas significativas. El modelo actual, basado en prueba y error de mecanismos terapéuticos, expone a los pacientes a meses de tratamiento ineficaz y pérdida de control de la enfermedad. El objetivo central es pasar de ese enfoque empírico a una predicción individualizada desde el inicio del tratamiento y mantenida a lo largo del tiempo.
Aunque existen biomarcadores diagnósticos y pronósticos, la autora destaca que el verdadero salto vendrá de los biomarcadores predictivos, capaces de vincular a cada paciente con un mecanismo patogénico y una estrategia de dosificación específicos antes de iniciar la terapia.
El objetivo central del nuevo paradigma es pasar de la experimentación empírica a la predicción individual desde el inicio del tratamiento y sostenerla longitudinalmente
Para ello, será necesario integrar datos multiómicos con fenotipado clínico detallado, imágenes, biomarcadores digitales, resultados reportados por los pacientes y datos longitudinales del mundo real, lo que permitirá definir subgrupos biológicos clínicamente accionables.
En este marco, los modelos computacionales y los gemelos digitales aparecen como herramientas clave para simular respuestas individuales y optimizar la selección y la dosis de los tratamientos. Estas firmas predictivas deberán ser válidas en distintas poblaciones y sistemas de salud, y evaluadas por su impacto clínico real, como reducción del tiempo hasta el control, menos tratamientos fallidos y mejor calidad de vida. La autora propone integrar estas herramientas en la práctica clínica mediante farmacogenómica, farmacotranscriptómica y diseños de ensayos adaptativos basados en biomarcadores.
El éxito de este desafío se medirá cuando los modelos predictivos, validados prospectivamente, permitan al clínico elegir la primera terapia correcta y guiar cuándo continuar, ajustar o cambiar el tratamiento, convirtiendo la precisión en una herramienta clínica tangible.
Segundo gran desafío: la traducción
La autora plantea que uno de los mayores cuellos de botella en el desarrollo de fármacos dermatológicos es la pobre traducción entre los modelos preclínicos y los resultados en pacientes. Muchos objetivos con sólida justificación genética y biológica fracasan en fases tempranas.
El ejemplo de RORγt en psoriasis ilustra este problema: pese a su fuerte respaldo mecanístico y al éxito del eje IL-17/IL-23, su inhibición con una molécula pequeña produjo beneficios clínicos modestos y problemas de seguridad, muy inferiores a los de los biológicos. Esto evidencia que los modelos preclínicos tradicionales no predicen de forma fiable la eficacia ni la seguridad humanas.
El problema radica en que los modelos más utilizados no reproducen la cronicidad, la arquitectura tisular ni la complejidad multicelular de la piel humana. Aunque la inteligencia artificial está acelerando la identificación de dianas y compuestos, sus predicciones solo son útiles si se validan en sistemas experimentales que reflejen biología humana real.

El problema radica en que los modelos más utilizados no reproducen la cronicidad, la arquitectura tisular ni la complejidad multicelular de la piel humana
Por ello, la autora propone priorizar modelos traslacionales más humanos: organoides cutáneos 3D, piel-en-chip, ratones humanizados y explantes de piel humana, que permiten evaluar compromiso del blanco, señalización y efectos farmacodinámicos en un microambiente cutáneo intacto. Integrar estos sistemas con farmacología traslacional, imagen y análisis espacial permite seleccionar dosis y esquemas que realmente correspondan al mecanismo de acción antes de entrar en clínica.
En paralelo, la autora subraya la necesidad de una validación rigurosa y transparente de los enfoques basados en IA, con estudios prospectivos, controles negativos, cegamiento y planes de análisis preregistrados. La estandarización regulatoria y el uso de materiales de referencia comunes serán claves para comparar y reproducir resultados.
Este desafío estará superado cuando los datos preclínicos predigan de forma consistente el éxito en fase II, cuando el compromiso del blanco se traduzca en biomarcadores clínicamente relevantes, y cuando menos fármacos fracasen en clínica porque el paquete preclínico sea realmente predictivo.
Tercer gran desafío: la modalidad
La autora sostiene que muchas de las dianas más relevantes en dermatología no son accesibles con las modalidades clásicas (moléculas pequeñas y anticuerpos).
Los principales impulsores de enfermedad —programas transcripcionales, interacciones proteína-proteína intracelulares y variantes genéticas— exigen nuevas plataformas terapéuticas, como terapias de ácidos nucleicos, edición génica, degradadores de proteínas, pegamentos moleculares, anticuerpos biespecíficos y sistemas celulares modificados.
La piel impone una paradoja: es una barrera potente, pero también un órgano accesible, que permite administración local, focalización y visualización directa de la respuesta. El ejemplo de ruxolitinib tópico muestra cómo un mecanismo sistémico puede convertirse en una terapia cutánea dirigida mediante innovación en formulación y entrega.
El progreso real dependerá de dominar la entrega dirigida a compartimentos cutáneos específicos (queratinocitos, melanocitos, fibroblastos, células inmunes, folículos) mediante microagujas, nanopartículas, vesículas, sistemas foliculares o inyección intradérmica, maximizando eficacia local y minimizando exposición sistémica. Estas plataformas también permiten reposicionar fármacos conocidos mejorando su perfil beneficio-riesgo sin cambiar la molécula activa.

La piel impone una paradoja: es una barrera potente, pero también un órgano accesible, que permite administración local, focalización y visualización directa de la respuesta
Para la autora, las modalidades avanzadas solo avanzarán si los estudios demuestran distribución tisular precisa, actividad en la diana y tolerabilidad, junto con paquetes de química, manufactura y control (CMC) suficientemente robustos para sostener estudios en humanos. El éxito se medirá cuando estas nuevas plataformas logren concentraciones terapéuticas selectivas en la piel, con modulación de vías específica y seguridad aceptable, haciendo viable que modalidades antes ajenas a la dermatología entren en clínica.
Cuarto gran desafío: la curación
El desafío más ambicioso es pasar de la supresión de síntomas a la modificación duradera de la enfermedad. La autora destaca que muchas dermatosis recaen porque la piel conserva una “memoria de enfermedad”, sostenida por células T residentes patógenas, células estructurales reprogramadas, circuitos neuroinmunes y marcas epigenéticas. Las terapias actuales controlan la inflamación, pero no eliminan estos programas tisulares.
Define como objetivo una remisión sostenida sin tratamiento durante al menos 12 meses, lo que requerirá borrar o reprogramar la memoria tisular y restaurar estados de piel sana, no solo bloquear citocinas.

El desafío más ambicioso es pasar de la supresión de síntomas a la modificación duradera de la enfermedad
Este enfoque se extiende más allá de las dermatosis inflamatorias:
- .En cancerización de campo, el reto es eliminar tanto las lesiones visibles como los clones subclínicos que predisponen al carcinoma, mediante terapias dirigidas al campo.
- En cáncer cutáneo, las inmunoterapias ya han demostrado que la modificación profunda del microambiente puede cambiar el pronóstico.
- En heridas crónicas, el problema es un tejido atrapado en inflamación, senescencia y fracaso regenerativo; aquí, medicina regenerativa, sustitutos cutáneos, células madre, vesículas y andamios extracelulares ofrecen rutas para reconstruir la arquitectura tisular.
Para lograr una verdadera curación, la autora propone mapear longitudinal y espacialmente la piel humana para identificar qué poblaciones celulares y programas deben eliminarse o reprogramarse. Los ensayos deberán integrar biomarcadores de recaída, reglas de retirada y definiciones reproducibles de remisión.
El éxito se medirá por control sostenido tras la retirada, firmas moleculares de piel sana, eliminación duradera de campos precancerosos y cierre estable de heridas con piel funcional, integrando inmunología, oncología y medicina regenerativa en un mismo marco terapéutico.
Conclusiones
Los desafíos de precisión, traducción, modalidad y curación son interdependientes y deben abordarse de manera integrada. Modelos más predictivos pueden mejorar el rendimiento del descubrimiento asistido por IA; nuevas modalidades y sistemas de entrega amplían el espectro de dianas accesibles en la piel humana; y los biomarcadores predictivos permiten ensayos más eficientes, capaces de evaluar si una intervención modifica realmente la enfermedad y no solo suprime los síntomas.
En conjunto, estos avances pueden desplazar la dermatología desde el control sintomático hacia la remisión sostenida sin tratamiento y, en subgrupos seleccionados, hacia estrategias verdaderamente curativas.
La autora subraya que las herramientas para enfrentar estos desafíos ya existen y hace un llamado a la comunidad académica, la industria y los responsables de políticas sanitarias a impulsar investigaciones ambiciosas, rigurosamente comprobables y centradas en el beneficio del paciente.
Dermatología de precisión: la nueva era
Fuente
Grada A. Grand challenges in dermatologic drug discovery: four priorities to transform skin disease treatment. Front. Drug Discov 2026;5.









