Revisión que destaca el rol de teplizumab en el retraso de la progresión al estadio clínico de la diabetes tipo 1 y su potencial en la prevención temprana de la enfermedad
Lugones Editorial©
La aparición de nuevas terapias capaces de retrasar o prevenir la diabetes tipo 1 representa una oportunidad significativa para modificar la trayectoria de esta enfermedad. En este contexto, Saleem et al. revisan el estado actual del teplizumab, un anticuerpo monoclonal humanizado anti-CD3, como intervención para frenar la progresión hacia la diabetes clínica.
La diabetes tipo 1 surge de un ataque autoinmune a las células beta pancreáticas, lo que conduce a la dependencia de insulina exógena para mantener los niveles de glucosa. En los últimos años, la investigación se ha centrado cada vez más en estrategias preventivas para personas con alto riesgo.
Teplizumab es la primera terapia modificadora de la enfermedad aprobada para este objetivo, diseñada para retrasar la progresión al estadio clínico en adultos y niños de 8 años o más diagnosticados en estadio 2 de la enfermedad.

Los ensayos clínicos han demostrado que teplizumab puede retrasar la progresión de la diabetes tipo 1 desde el estadio 2 al 3 hasta por 2 años
Introducción
La diabetes es la enfermedad crónica no transmisible más frecuente, que actualmente afecta a aproximadamente 420 millones de personas en todo el mundo, con estimaciones que sugieren un aumento a 640 millones para 2040.
Entre los dos tipos principales, la DM1 generalmente se presenta en la infancia o la adolescencia, y representa aproximadamente el 80% de los nuevos diagnósticos en personas de 19 años o menos.
La progresión autoinmune en la DM1 se desarrolla en etapas distintas:
- La etapa 1 se caracteriza por la presencia de dos o más anticuerpos, típicamente contra el citoplasma de las células de los islotes, la descarboxilasa de glutamato, el antígeno del insulinoma 2 o el transportador de zinc 8, sin niveles anormales de glucosa.
- Esto avanza a la etapa 2, que se caracteriza por la disglucemia con la persistencia de dos o más autoanticuerpos.
- Y finalmente llega a la etapa 3, donde emergen síntomas característicos de la diabetes, incluyendo cetoacidosis diabética, polidipsia, polifagia, poliuria y pérdida de peso.
¿Cómo se produce la diabetes tipo 1?
La DM1 se desarrolla por una respuesta inmune dirigida contra las células β pancreáticas, mediada por células T CD4+ y CD8+, y células B. Las células T CD8+ son las principales responsables de la destrucción de las células β. Los precursores de células T se generan en la médula ósea y migran al timo, donde atraviesan la selección negativa, un proceso que elimina linfocitos autorreactivos y permite distinguir los antígenos propios de los extraños.
Posteriormente, las células T circulan por el torrente sanguíneo hasta los ganglios linfáticos, donde interactúan con péptidos específicos. En la DM1, los péptidos de células β son presentados por células presentadoras de antígenos (APC) a linfocitos T CD4+ autorreactivos en los ganglios pancreáticos.
Durante el desarrollo de la enfermedad, las células inmunitarias se infiltran en el páncreas, atacando las células β productoras de insulina y generando un entorno inflamatorio denominado insulitis. Esta inflamación favorece la progresión de la enfermedad al aumentar la presentación de antígenos de los islotes mediante moléculas HLA de clase I y facilitar la migración de células T activadas hacia los islotes, donde comienzan la destrucción de las células β.
El daño se potencia por citoquinas proinflamatorias liberadas por monocitos, células NK, neutrófilos y macrófagos.
Durante el desarrollo de la enfermedad, las células inmunitarias se infiltran en el páncreas, atacando las células β productoras de insulina y generando un entorno inflamatorio
En condiciones normales, las células T autorreactivas son eliminadas por mecanismos de tolerancia periférica, principalmente mediadas por células T reguladoras (Tregs). Defectos en la función de Tregs aumentan el daño de las células β. Además, la activación de células T puede estimular células B, provocando producción de autoanticuerpos contra proteínas de células β, que sirven como biomarcadores esenciales para el diagnóstico y seguimiento de la progresión de la T1D.
Terapias actuales: limitaciones
Los tratamientos convencionales para la DM1 se centran principalmente en la insulina exógena de por vida y algunos fármacos para optimizar la glucemia.
Aunque los regímenes de insulina han mejorado, estas terapias solo ofrecen alivio sintomático y no modifican la patogénesis subyacente ni mejoran los resultados a largo plazo.
Por ello, la investigación se ha orientado hacia estrategias preventivas en personas de alto riesgo, donde la terapia inmunomoduladora temprana puede preservar la función de las células β pancreáticas protegiéndolas del ataque autoinmune.

Se busca que la terapia inmunomoduladora temprana puede preservar la función de las células β pancreáticas protegiéndolas del ataque autoinmune
Teplizumab: acción sobre la diabetes tipo 1 en su origen
El teplizumab es un anticuerpo monoclonal humanizado anti-CD3 y la primera terapia modificadora de la enfermedad aprobada por la FDA para la DM1. Está diseñado para retrasar la progresión al estadio 3 en adultos y adolescentes ya en estadio 2. Su acción inmunomoduladora se produce mediante:
- Aumento de la proporción de células T reguladoras (Tregs).
- Depleción de células T CD8+ y CD4+ autorreactivas, desactivando linfocitos T responsables de la destrucción de células β.
- Inducción de apoptosis de células T activadas y modulación de la señalización a través de TGF-β y TNF-α.
- Cambio en la migración de células T y ajuste de mecanismos tolerogénicos.
- Promoción de células T CD4+FoxP3+ que reducen la producción de citoquinas proinflamatorias (IL-2, IFN-γ) y aumentan citoquinas antiinflamatorias (IL-4, IL-10).
Estos efectos combinados sugieren que el teplizumab puede moderar la respuesta inmune, proteger las células β y ralentizar la progresión de la DM1.
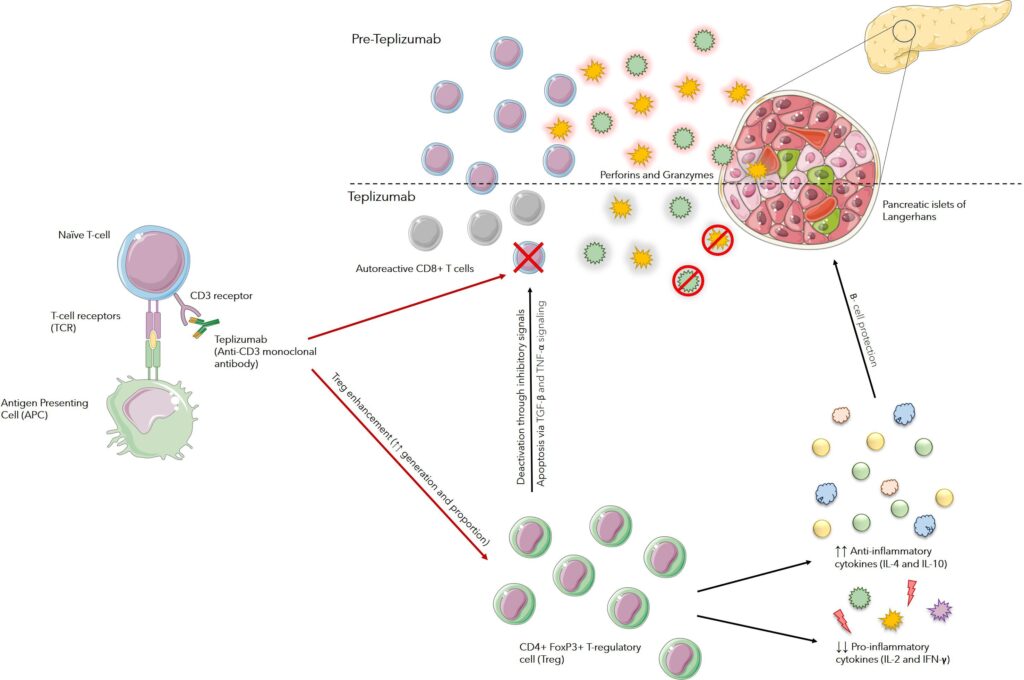
Mecanismo de acción del teplizumab
Ensayos clínicos de teplizumab: eficacia en la diabetes tipo 1
Durante los últimos 20 años, múltiples estudios clínicos han evaluado el teplizumab en individuos con DM1 en estadio 2 y 3, demostrando retención de la función de las células β, medida mediante péptido C.
- En un ensayo de fase 2, aleatorizado, controlado con placebo y doble ciego, se incluyó a 76 participantes de 8 años o más con alto riesgo de desarrollar DM1. Se administró un curso único de 14 días de teplizumab o placebo, y la progresión a DM clínica se evaluó mediante pruebas de tolerancia a la glucosa cada 6 meses. Tras un seguimiento medio de 51 meses, solo el 43% de los tratados con teplizumab progresaron al estadio 3, frente al 72% del grupo placebo. El tiempo medio hasta el diagnóstico fue significativamente mayor en el grupo de teplizumab (48,4 vs. 24,4 meses; cociente de riesgo 0,41, IC 95% 0,22-0,78, P = 0,006). El efecto más marcado se observó durante el primer año: 7% de diagnóstico en teplizumab frente a 44% en placebo.
- En un ensayo de extensión con seguimiento medio de 76,9 meses, la mediana hasta el diagnóstico fue de 59,6 meses para teplizumab y 27,1 meses para placebo; el 50% de los tratados permanecieron libres de diabetes frente al 22 % del placebo.
- En una fase 3 con 328 niños y adolescentes, el grupo de teplizumab mostró mayores niveles de péptido C estimulado a la semana 78, aunque no se observaron diferencias en hemoglobina glucosilada, dosis de insulina o eventos hipoglucémicos anuales.
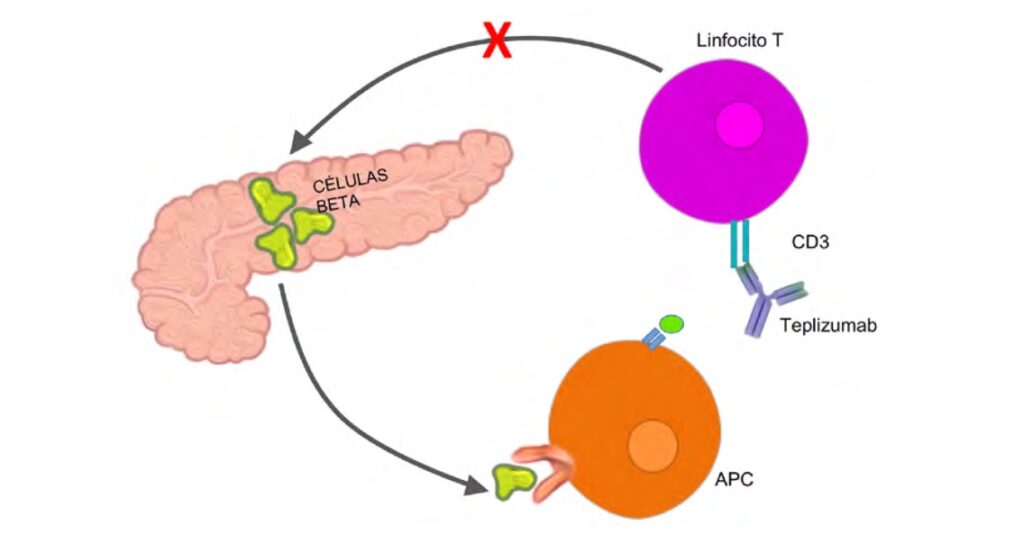
Teplizumab modula la respuesta inmune al bloquear y alterar la función de los linfocitos T CD3+, promoviendo la tolerancia inmunológica y reduciendo la destrucción autoinmune de las células beta pancreáticas. En la imagen, mecanismo de acción del anticuerpo anti-CD3.
Seguridad y efectos secundarios
Los efectos adversos más frecuentes (>10%) incluyeron: linfopenia (73%), erupción (36%), leucopenia (21%) y cefalea (11%). Se debe premedicar y monitorear el síndrome de liberación de citoquinas (SRC), que afectó al 5 % de los pacientes tratados, frente al 0,8 % en placebo, con síntomas como fiebre, náuseas, fatiga, dolor de cabeza, mialgia, artralgia y elevación de enzimas hepáticas (ALT, AST, bilirrubina).
El teplizumab debe suspenderse si los niveles de ALT o AST superan cinco veces el límite superior normal, y se debe pausar el tratamiento ante un SRC grave. Está contraindicado en infecciones graves activas, y el tratamiento debe interrumpirse si surge alguna infección significativa.
Discusión
La aparición de terapias como el teplizumab, capaces de retrasar o prevenir la DM1, representa una oportunidad importante para modificar la trayectoria de la enfermedad. Una encuesta realizada a 95 padres de niños con DM1, que además tenían al menos otro hijo sin la condición, mostró que solo el 6,3% tenía un conocimiento detallado sobre teplizumab, aunque el 52,6% estaba dispuesto a aprobar su uso si su hijo cumplía los criterios de elegibilidad.
Respecto de los beneficios percibidos, el 62,1% informó una reducción del estrés familiar, el 40% mencionó la prevención de cetoacidosis diabética (CAD) y el 27,4% destacó una mayor preparación para manejar la DM. Las respuestas emocionales fueron mixtas: el 53,7 % expresó esperanza, mientras que el 52,6 % expresó preocupación por posibles efectos emocionales negativos durante la administración.
Aunque se han reportado eventos adversos transitorios, como linfopenia, erupción y síndrome de liberación de citoquinas, el perfil de seguridad general del teplizumab parece favorable, especialmente comparado con terapias inmunosupresoras convencionales previas, como azatioprina, ciclosporina o prednisona, que ofrecen mejoras temporales, pero con riesgos significativos a largo plazo.

La aparición de terapias como el teplizumab representa una oportunidad importante para modificar la trayectoria de la enfermedad
Actualmente, el uso clínico se limita a familiares de individuos con DM1 que presentan disglucemia y dos o más autoanticuerpos de islote, pero aún no han desarrollado diabetes manifiesta.
Se requieren más estudios en poblaciones amplias y diversas, especialmente pediátricas menores de 8 años, para definir completamente los beneficios, riesgos, régimen de dosificación, duración y momento óptimo de administración.
A pesar de estas incertidumbres, los avances hasta la fecha generan expectativas de un futuro en que la DM1 no implique necesariamente dependencia de insulina de por vida.

Los avances hasta la fecha generan expectativas de un futuro en que la diabetes tipo 1 no implique necesariamente dependencia de insulina de por vida
Conclusiones
Más allá del tratamiento, se debe enfatizar la detección temprana de la DM1, identificando etapas presintomáticas mediante autoanticuerpos de islote en individuos en riesgo.
Esta estrategia reduce notablemente el riesgo de CAD al momento del diagnóstico (tasas menores al 5 % frente a 15-80 % en individuos no examinados), permite a familias y profesionales planificar el manejo, proporciona alivio emocional, abre la posibilidad de intervenciones terapéuticas, preserva la función de las células β y mejora los resultados a largo plazo.

La detección temprana de la diabetes tipo reduce notablemente el riesgo de cetoacidosis diabética
Teplizumab y diabetes tipo 1
Fuente
Saleem MR, Khan MH. Teplizumab: a promising intervention for delaying type 1 diabetes progression. Front Endocrinol 2025;16.