La generación de células beta funcionales a partir de células madre, junto con avances en encapsulación, inmunomodulación y bioingeniería, redefine las terapias celulares en diabetes tipo 1 como una estrategia potencialmente curativa, aunque aún limitada por desafíos de inmunogenicidad, costo y escalabilidad
Lugones Editorial©
En los últimos años se ha producido un cambio en el escenario de las terapias celulares en diabetes tipo 1 que representa un avance transformador en la búsqueda de un tratamiento curativo para la enfermedad. A pesar de los avances en los sistemas de administración de insulina y el monitoreo de la glucosa, lograr un control glucémico estricto sigue siendo un desafío para muchos pacientes.
En este contexto, la generación de células β derivadas de células madre ha emergido como una estrategia prometedora para restaurar la producción de insulina endógena.
Esta revisión se centra en los avances en la diferenciación de células madre pluripotentes humanas -incluyendo células madre embrionarias e iPSC- hacia células β funcionales, así como en la mejora de su madurez, supervivencia y protección inmunológica.
Además, aborda las principales estrategias de trasplante y encapsulación, junto con la evidencia clínica disponible, y analiza las limitaciones actuales, como el rechazo inmune, la desdiferenciación celular y los desafíos de seguridad. Finalmente, explora las perspectivas futuras, incluyendo la edición génica, la personalización terapéutica y la integración de inteligencia artificial.
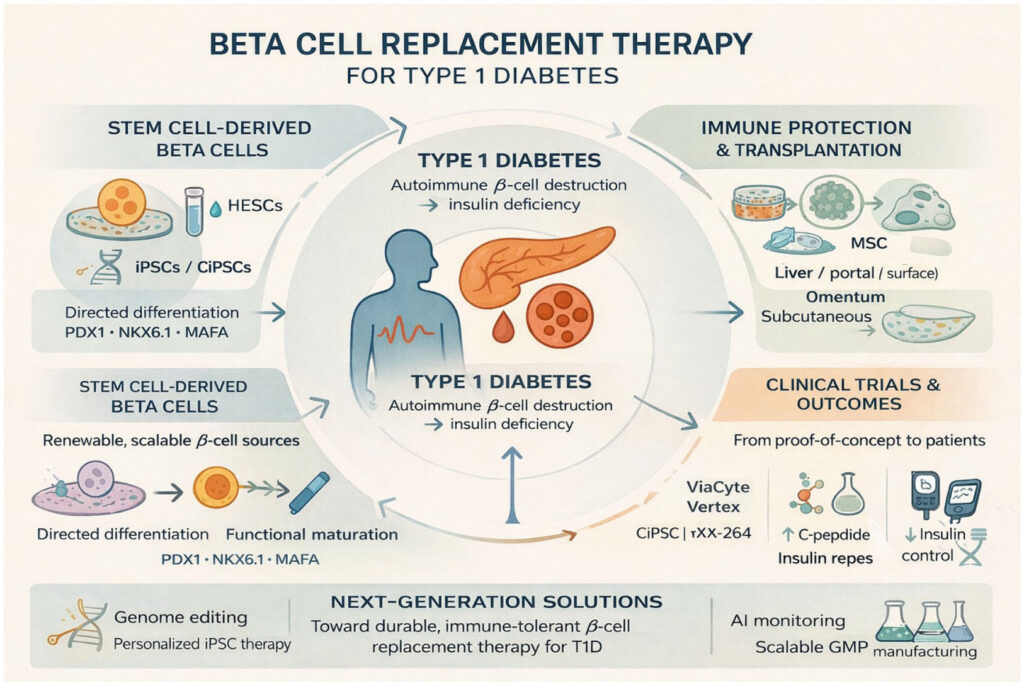
Resumen de cómo se generan las células β derivadas de células madre, protegidas del rechazo inmunológico y traducidas en terapias clínicas para la diabetes tipo 1
Introducción
La diabetes tipo 1 es una enfermedad autoinmune caracterizada por la destrucción de las células β y la dependencia de insulina exógena, que no logra reproducir la homeostasis glucémica fisiológica ni prevenir completamente las complicaciones a largo plazo. Si bien el trasplante de islotes ha demostrado eficacia, su uso está limitado por la escasez de donantes y la necesidad de inmunosupresión.
En este contexto, las terapias con células β derivadas de células madre han avanzado desde estudios experimentales hacia ensayos clínicos en humanos, demostrando injerto y producción de insulina endógena. Estos progresos se apoyan en mejoras en la diferenciación celular, la protección inmunológica y las estrategias de trasplante, aunque persisten desafíos relevantes como la inmunogenicidad, la maduración incompleta, la seguridad y los costos.

Evolución de la terapia con células beta derivada de células madre
Fuentes de células madre: plataforma del reemplazo beta
Las terapias celulares en DM1 se basan en la generación de células β funcionales capaces de restaurar la secreción de insulina, utilizando células madre pluripotentes humanas como principal plataforma. Las células madre embrionarias (hESC) constituyen la fuente más robusta, con alta eficiencia de diferenciación hacia células productoras de insulina, aunque su aplicación clínica está limitada por barreras éticas e inmunológicas.
Las células madre pluripotentes inducidas (iPSC) emergen como una alternativa clave, con potencial autólogo y menor inmunogenicidad, aunque presentan desafíos en términos de variabilidad entre líneas y maduración funcional. En conjunto, ambas plataformas reflejan la transición hacia fuentes celulares escalables para reemplazo beta.
- Diferenciación dirigida: imitar el desarrollo pancreático
La diferenciación de células madre hacia células β reproduce etapas del desarrollo embrionario, desde endodermo definitivo hasta células maduras, mediante la regulación precisa de vías de señalización y factores de transcripción. La generación de progenitores pancreáticos PDX1+/NKX6.1+ y la activación de NEUROG3 son puntos críticos para lograr identidad y función beta.
A pesar de los avances, la eficiencia sigue limitada por la heterogeneidad celular y la incapacidad de reproducir completamente el microambiente pancreático.
- Maduración y escalabilidad: el cuello de botella
Aunque se logran células productoras de insulina, la maduración funcional completa -con secreción adecuada de insulina dependiente de glucosa- continúa siendo un desafío, requiriendo maduración prolongada in vitro o in vivo.
La escalabilidad clínica está restringida por limitaciones en producción bajo estándares GMP, variabilidad entre lotes, criopreservación y falta de métricas estandarizadas de calidad.
- Nuevas plataformas: hacia mayor reproducibilidad
Los sistemas tridimensionales, biorreactores y organoides han mejorado la diferenciación y funcionalidad celular al reproducir mejor el microambiente. En paralelo, se desarrollan ensayos de potencia y control de calidad estandarizados, necesarios para la validación regulatoria y la aplicación clínica.
- Otras fuentes celulares: rol complementario
Las MSC no generan células β, pero cumplen un rol inmunomodulador y de soporte, mejorando el injerto y la supervivencia celular. Las células progenitoras adultas tienen una capacidad limitada de diferenciación y un papel principalmente indirecto.
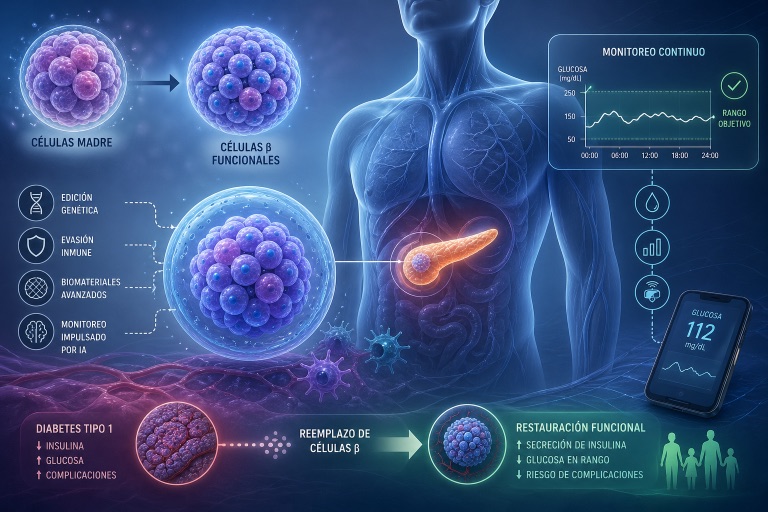
Las distintas fuentes celulares están impulsando la transición hacia terapias de reemplazo de células β clínicamente viables, acercando la restauración funcional de la secreción de insulina.
Maduración funcional: requisito para eficacia clínica
La obtención de células β derivadas de células madre no garantiza su funcionalidad completa. Si bien los protocolos actuales logran células productoras de insulina, muchas no reproducen la fisiología de las células β nativas, lo que limita su aplicación clínica.
- Marcadores de madurez
La maduración se evalúa mediante la expresión conjunta de marcadores clave, como PDX1, NKX6.1, MAFA e insulina, asociados al desarrollo, identidad y capacidad de respuesta a la glucosa. Su coexpresión indica una mayor competencia funcional.
- Evaluación funcional in vitro
La funcionalidad se determina principalmente mediante ensayos de secreción de insulina estimulada por glucosa (GSIS), donde una respuesta dependiente de la glucosa refleja maduración adecuada.
De forma complementaria, los estudios de flujo de calcio permiten evaluar el acoplamiento estímulo-secreción, evidenciando la capacidad de respuesta celular.
- Brecha con la célula β nativa
A pesar de los avances, las células derivadas de células madre muestran una funcionalidad inferior a los islotes humanos, con menor secreción de insulina, respuesta retardada y persistencia de rasgos inmaduros.
El microambiente juega un rol clave: sistemas más complejos, como matrices biomiméticas o vascularizadas, mejoran la respuesta a la glucosa y la dinámica secretora, acercándose a un comportamiento fisiológico.
Métodos de entrega y trasplante: más que implantar células
El éxito de las terapias celulares en DM1 no depende solo de generar células β funcionales, sino de cómo y dónde se trasplantan. La elección del sitio y las estrategias de entrega condicionan la supervivencia, la oxigenación y la función del injerto a largo plazo.
- Sitios de trasplante: equilibrio entre acceso y oxigenación
La vía intraportal hepática sigue siendo el estándar clínico, con buena vascularización, pero limitada por inflamación temprana (IBMIR) y pérdida progresiva del injerto.
El sitio subcutáneo es más seguro y accesible, aunque su baja oxigenación compromete la viabilidad celular.
Como alternativas, el omento y la superficie hepática muestran mejores condiciones de oxigenación y revascularización, posicionándose como opciones prometedoras. Otros sitios (intramuscular, subcapsular renal) continúan en evaluación.
- Encapsulación: protección inmunológica del injerto
Las tecnologías de encapsulación permiten aislar las células del sistema inmune manteniendo el intercambio de nutrientes e insulina.
. Macroencapsulación: dispositivos implantables recuperables, pero limitados por difusión de oxígeno.
. Microencapsulación: mejor intercambio metabólico, aunque con riesgo de fibrosis y pérdida funcional.
- Oxigenación y biomateriales: determinantes del éxito
La hipoxia es una limitación central. Para superarla, se desarrollan biomateriales proangiogénicos, sistemas liberadores de oxígeno y matrices prevascularizadas, que mejoran la integración vascular y la función del injerto.
- Plataformas de entrega: hacia microambientes diseñados
Los andamios e hidrogeles permiten organizar las células en 3D, favorecer la vascularización y replicar el microambiente pancreático. Estas estrategias integran soporte estructural, protección inmune y optimización metabólica.
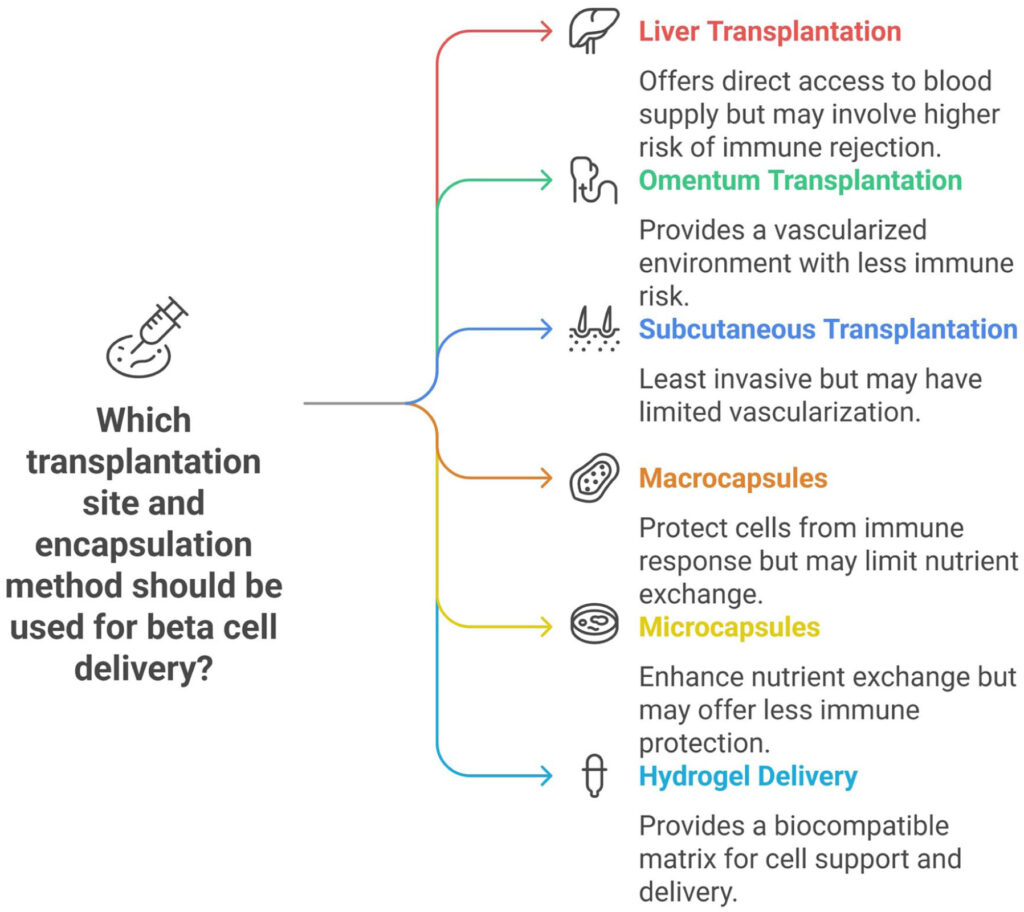
Rutas de entrega y dispositivos de encapsulación
Desafíos inmunológicos: la barrera crítica
El rechazo inmunológico sigue siendo uno de los principales obstáculos para las terapias celulares en DM1, afectando tanto a trasplantes alogénicos como autólogos. Intervienen mecanismos de aloinmunidad, autoinmunidad recurrente y respuestas inflamatorias del huésped, que condicionan la pérdida del injerto.
- Alogénico vs autólogo
El trasplante autólogo (iPSC) reduce el rechazo, pero es costoso, complejo y no elimina el riesgo de autoinmunidad.
El enfoque alogénico es más escalable, aunque requiere estrategias de modulación inmune para evitar el rechazo.
- Respuesta inmune del huésped
Tras el trasplante, se activan tanto la inmunidad innata (inflamación precoz) como la adaptativa (citotoxicidad mediada por células T), con impacto en la supervivencia a corto y largo plazo. En DM1, además, puede reactivarse la autoinmunidad contra las células β.
- Evasión inmune: hacia injertos “invisibles”
Las estrategias actuales buscan evitar la inmunosupresión sistémica mediante:
. Edición génica: eliminación de HLA y sobreexpresión de moléculas como PD-L1 o CD47 para reducir el reconocimiento inmune.
. Encapsulación y biomateriales: barreras físicas que limitan la infiltración inmune sin afectar el intercambio metabólico.
. Coterapias celulares (MSC): modulación local de la respuesta inmune y mejora del injerto.
En este contexto, la tendencia actual es hacia una ingeniería inmune multimodal, que combine modificaciones celulares y estrategias locales para lograr tolerancia inmunológica sin inmunosupresión sistémica.
Ensayos clínicos e hitos traslacionales
En la última década, las terapias con células β derivadas de células madre han avanzado de la prueba de concepto preclínica a ensayos clínicos en humanos, con evidencia de restauración de la secreción de insulina, aumento de péptido C, reducción significativa de los requerimientos de insulina exógena y, en algunos casos, independencia parcial o completa de insulina.
Los programas clínicos han marcado hitos relevantes. Los dispositivos de progenitores pancreáticos encapsulados demostraron seguridad e injerto, aunque limitados por fibrosis pericapsular y difusión insuficiente de oxígeno.
En paralelo, terapias con células β completamente diferenciadas administradas por vía intraportal lograron mejoras metabólicas robustas e independencia de insulina en subgrupos, aunque bajo inmunosupresión.
Asimismo, estrategias más recientes basadas en iPSC autólogas han mostrado restauración de péptido C y reducción de HbA1c sin inmunosupresión crónica, aunque con eficacia aún parcial.
- Alcances y límites actuales
En conjunto, estos ensayos confirman la viabilidad del reemplazo celular en humanos y marcan la transición hacia terapias clínicamente aplicables. Sin embargo, persisten limitaciones clave, incluyendo la durabilidad del injerto, la necesidad de inmunosupresión en algunos enfoques, la optimización del sitio de trasplante y la escalabilidad de la producción. Estos desafíos continúan definiendo el camino hacia una implementación clínica sostenida.

Si bien se confirma la viabilidad del reemplazo celular en humanos, aún persisten limitaciones clave, incluyendo la durabilidad del injerto, la necesidad de inmunosupresión en algunos enfoques, la optimización del sitio de trasplante y la escalabilidad de la producción
Limitaciones y desafíos actuales
A pesar de su potencial transformador, la terapia con células β derivadas de células madre enfrenta barreras relevantes de escalabilidad, costo y regulación que limitan su implementación clínica.
La producción bajo estándares GMP sigue siendo compleja, con protocolos prolongados (>30 días), rendimientos variables y costos elevados por lote, lo que dificulta su aplicación a gran escala. A esto se suman desafíos logísticos, como la criopreservación, donde la viabilidad y funcionalidad celular pueden verse comprometidas tras el descongelamiento, impactando la distribución y almacenamiento.
Desde el punto de vista económico, los costos estimados por paciente son altos, comparables a trasplantes de páncreas o islotes, lo que plantea interrogantes sobre acceso y sostenibilidad, aunque podrían compensarse a largo plazo si se logra independencia de insulina y reducción de complicaciones.
Finalmente, la complejidad regulatoria, la variabilidad entre lotes y las preocupaciones de seguridad (incluyendo riesgo tumorigénico y estabilidad a largo plazo) siguen siendo obstáculos críticos. En conjunto, la adopción clínica requerirá integrar eficacia biológica con fabricación reproducible, marcos regulatorios claros y modelos de costo-efectividad viables.
Tecnologías emergentes y direcciones futuras
El futuro del reemplazo de células β se orienta hacia la integración de bioingeniería, edición génica y herramientas computacionales para mejorar la durabilidad y personalización del tratamiento.
El monitoreo del injerto impulsado por inteligencia artificial, combinado con sensores continuos de glucosa y modelos predictivos (“gemelos digitales”), permite detectar precozmente la disfunción y optimizar la respuesta terapéutica. En paralelo, la integración multiómica mejora la caracterización celular y el emparejamiento donante-receptor, favoreciendo productos más estandarizados.
Las estrategias de edición génica buscan generar células β hipoinmunogénicas mediante la modulación de HLA y la expresión de moléculas inmunorreguladoras, mientras que los avances en biomateriales y andamios vascularizados mejoran la oxigenación, la integración y la supervivencia del injerto.
En conjunto, estas innovaciones apuntan a transformar el reemplazo de células β en una terapia de precisión, más duradera y potencialmente curativa, aunque su implementación dependerá de resolver los desafíos de escalabilidad, seguridad y regulación.
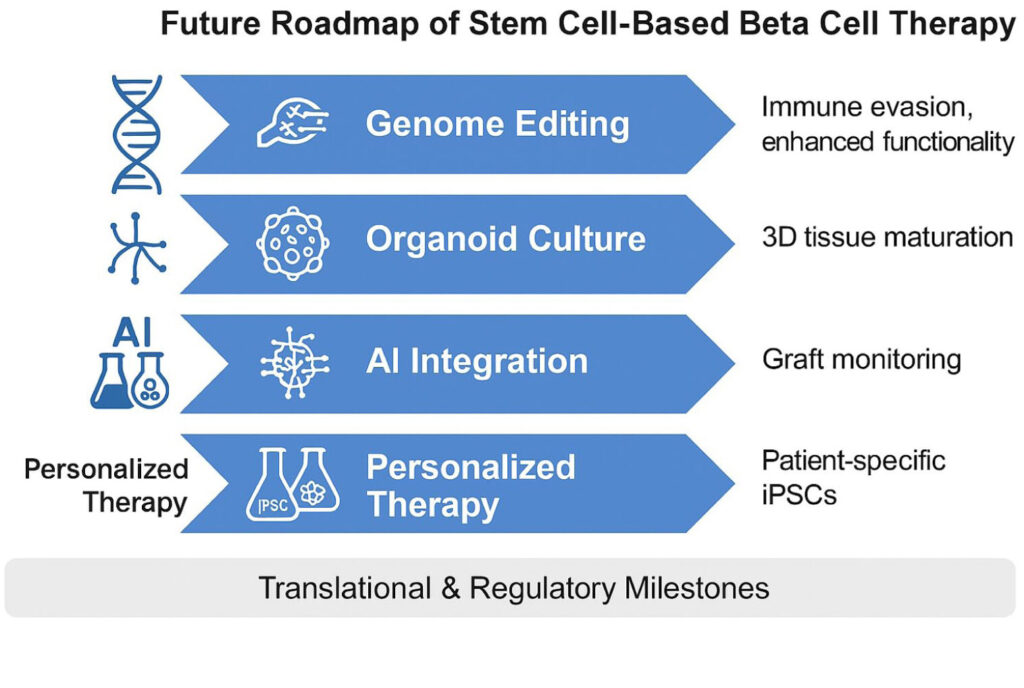
Hoja de ruta futura de la terapia con células beta basada en células madre
Conclusiones
Las terapias celulares en diabetes tipo 1, basadas en células β derivadas de células madre, representan uno de los avances más relevantes hacia un enfoque potencialmente curativo. En la última década, la mejora en los protocolos de diferenciación, las estrategias de inmunomodulación y las tecnologías de encapsulación ha permitido una transición concreta hacia la evaluación clínica en humanos.
Sin embargo, la implementación a gran escala sigue limitada por desafíos persistentes, incluyendo la inmunogenicidad, los altos costos de producción y la complejidad regulatoria. En este contexto, la traducción efectiva requerirá integrar de manera estratégica la biología de células madre con la bioingeniería y las innovaciones computacionales.
El futuro del campo se orienta hacia enfoques multidisciplinarios que combinan edición génica, monitoreo impulsado por inteligencia artificial y caracterización multiómica, con el objetivo de lograr injertos duraderos, funcionales e inmunotolerantes. En definitiva, el éxito clínico dependerá no solo de generar células β funcionales, sino de construir un ecosistema terapéutico integrado, capaz de llevar el reemplazo celular desde la eficacia experimental hacia un beneficio sostenido en la práctica clínica.
Las terapias celulares en diabetes tipo 1, basadas en células β derivadas de células madre, representan uno de los avances más relevantes hacia un enfoque potencialmente curativo
Terapias celulares en diabetes tipo 1
Fuente
Upadhye KS, Tayade P. Advances in stem cell-derived beta-cell therapy: A new frontier in type 1 diabetes treatment. Cell Transplant 2026;35:9636897261417623.