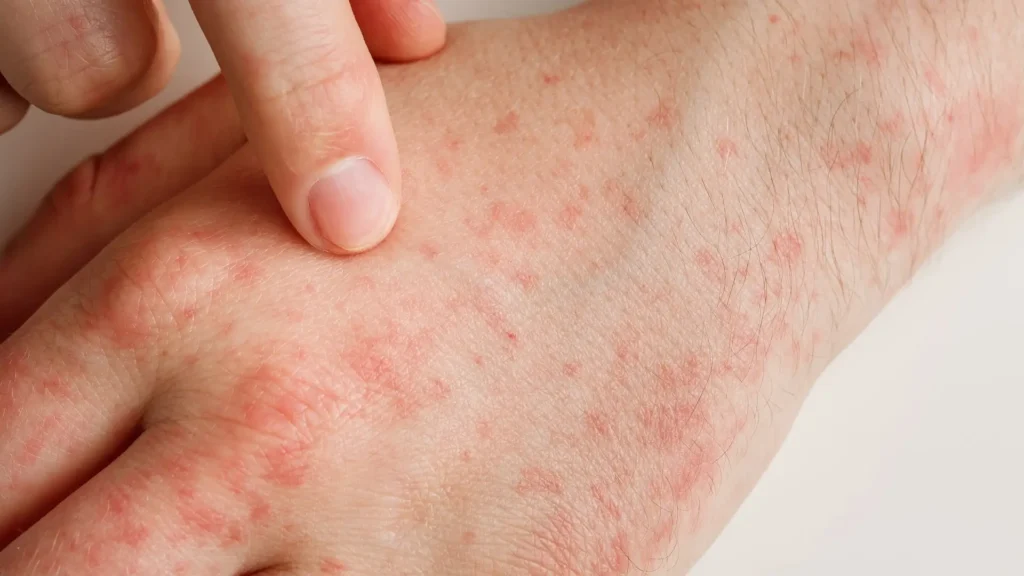
Revisión que analiza el espectro de las manifestaciones cutáneas relacionadas con el gluten más allá de la dermatitis herpetiforme, con especial foco en otras dermatosis asociadas
Lugones Editorial©
Los trastornos relacionados con el gluten (gluten-related disorders, GRDs) constituyen un amplio espectro de entidades inmunomediadas desencadenadas por la ingestión de gluten. Dentro de este marco, las manifestaciones cutáneas representan una dimensión clínica relevante que va más allá de la clásica dermatitis herpetiforme (DH), objeto central de esta revisión.
La enfermedad celíaca (celiac disease, CD) es la entidad mejor caracterizada dentro de los GRDs. El término sensibilidad al gluten incluye el conjunto de GRDs, abarcando tanto los casos con positividad serológica para anticuerpos relacionados con el gluten como aquellos sin síntomas gastrointestinales manifiestos.
La asociación entre la CD y la DH, considerada la manifestación cutánea específica de la CD, es la más ampliamente reconocida. No obstante, en los últimos años se han descrito otras manifestaciones cutáneas vinculadas a la CD, entre ellas psoriasis, dermatitis atópica (DA) y urticaria crónica.
Asimismo, también se han reportado manifestaciones cutáneas en pacientes con sensibilidad al gluten no celíaca (non-celiac gluten sensitivity, NCGS), entidad caracterizada por síntomas desencadenados por la ingestión de gluten que mejoran con la dieta libre de gluten (gluten-free diet, GFD).
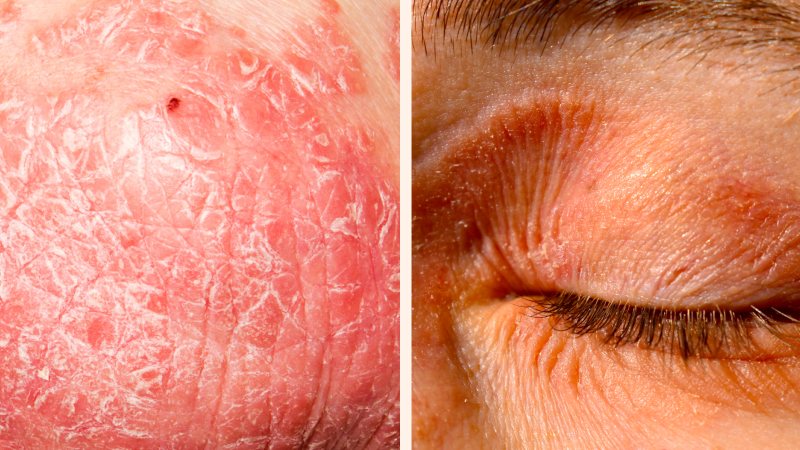
En los últimos años se han descrito otras manifestaciones cutáneas vinculadas a la enfermedad celíaca, entre ellas psoriasis, dermatitis atópica y urticaria crónica
Dermatitis herpetiforme
Descrita en 1884 por Duhring, la dermatitis herpetiforme (DH) es una dermatosis ampollar intensamente pruriginosa caracterizada por pápulas y pequeñas vesículas agrupadas en patrón herpetiforme. Actualmente se reconoce como la manifestación cutánea específica de la CD dentro del espectro de los GRDs.
Inmunopatogenia: eje TG2–TG3
El avance clave en la comprensión de la DH fue la identificación de inmunoglobulina A (IgA) como mediador central y, posteriormente, del autoantígeno epidérmico principal: la transglutaminasa 3 (TG3).
Las transglutaminasas constituyen una familia de nueve enzimas con expresión tisular diferencial; mientras TG2 y TG7 se expresan de forma ubicua, TG1, TG2, TG3 y TG5 se expresan en piel, principalmente en epidermis. En la CD, la gliadina desamidada por TG2 en intestino aumenta su antigenicidad y desencadena la producción de autoanticuerpos contra TG2.
En la DH, además de anti-TG2, se generan autoanticuerpos IgA contra TG3, que se depositan en forma granular en las puntas papilares dérmicas, hallazgo característico en la inmunofluorescencia directa (DIF).
Un punto relevante es que, aunque tanto CD como DH presentan autoanticuerpos contra TG2 y TG3, solo en la DH se detectan depósitos cutáneos granulares de IgA dirigidos contra TG3. Se postula que la exposición crónica al gluten favorecería un fenómeno de “propagación de epítopos” que explicaría la transición desde la enteropatía a la expresión cutánea. Clínicamente, esto es coherente con el hecho de que la CD suele preceder al desarrollo de DH.
También se han descrito autoanticuerpos contra TG6 en algunos pacientes.
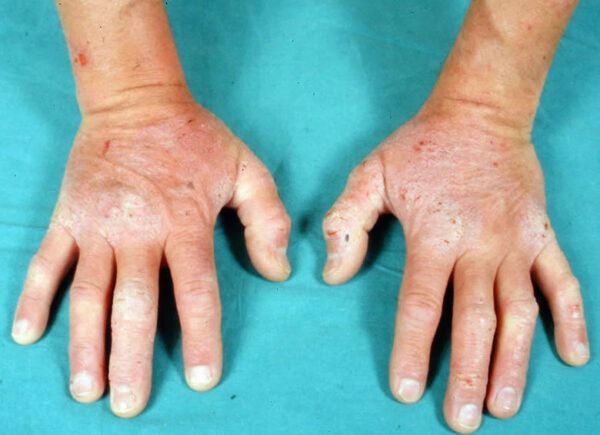
En la dermatitis herpetiforme, además de anti-TG2, se generan autoanticuerpos IgA contra TG3, que se depositan en forma granular en las puntas papilares dérmicas
Prurito: más que histamina
La fisiopatología del prurito en la DH no está completamente aclarada. Se han implicado mecanismos de inflamación neurogénica, con participación de sustancia P, desgranulación mastocitaria y liberación de citocinas (IL-1, IL-6, IL-8). Además, la IL-31 —asociada a dermatosis pruriginosas con perfil Th2— se encuentra elevada en suero y piel de pacientes con DH. También se ha reportado sobreexpresión de linfopoyetina estromal tímica y distintos neuropéptidos cutáneos, lo que sugiere una red neuroinmunológica compleja más allá de la simple activación histamínica.
Este enfoque es particularmente relevante para dermatólogos, dado que posiciona a la DH dentro del grupo de dermatosis pruriginosas inmunomediadas con componentes Th2 y neuroinflamatorios.
Epidemiología y diagnóstico
La DH es una enfermedad rara, predominante en poblaciones caucásicas, en estrecha relación con la presencia de HLA-DQ2 y HLA-DQ8.
Un dato interesante es que, mientras la incidencia de CD ha aumentado en las últimas décadas, la incidencia de DH ha disminuido, posiblemente debido al diagnóstico y tratamiento más precoz de la CD.
Desde el punto de vista dermatológico, la DH debe diferenciarse de otras enfermedades ampollares autoinmunes y de dermatosis pruriginosas no autoinmunes como sarna o foliculitis diseminada, lo que refuerza la importancia de la inmunofluorescencia directa como herramienta diagnóstica clave.
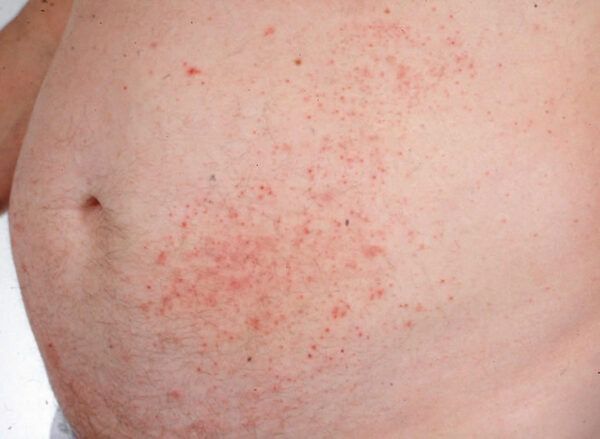
Mientras la incidencia de la enfermedad celíaca ha aumentado en las últimas décadas, la incidencia de la dermatitis herpetiforme ha disminuido
Presentación clínica
La DH presenta un patrón clínico característico. Las lesiones primarias consisten en pápulas eritematosas agrupadas con pequeñas vesículas superpuestas, dispuestas en patrón herpetiforme. Sin embargo, el prurito intenso —síntoma cardinal de la enfermedad— suele condicionar excoriaciones y erosiones secundarias que pueden enmascarar la morfología vesicular típica.
La ausencia de prurito hace poco probable el diagnóstico de DH.
La distribución es típicamente simétrica y predomina en superficies extensoras, especialmente codos y rodillas, así como en cuello y región glútea. También puede afectar cara, región frontal del cuero cabelludo e ingle. Las lesiones suelen resolverse sin cicatriz, aunque es frecuente la hiper o hipopigmentación postinflamatoria.
La afectación mucosa es rara, pero se han descrito máculas eritematosas y erosiones orales acompañadas de dolor o sensación urente. Asimismo, se han reportado anomalías dentales, incluyendo surcos horizontales, alteraciones del color del esmalte y pitting.
En pacientes pediátricos —y raramente en adultos— pueden observarse petequias palmoplantares asintomáticas, predominantemente en la extremidad dominante. También se han descrito de forma anecdótica variantes con queratosis palmoplantar o lesiones semejantes a prurigo pigmentosa.
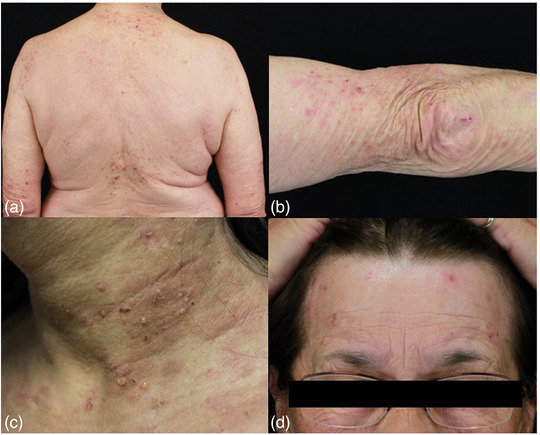
Características clínicas de la dermatitis herpetiforme. A) Pápulas eritematosas agrupadas dispuestas en un patrón herpetiforme. B) Excoriación de la piel debido a un prurito intenso, típico de la dermatitis herpetiforme. C)Pequeñas ampollas en la piel eritematosa en un paciente con fototipo V según la clasificación de fototipo de Fitzpatrick. D) Excoriaciones en la frente
Diagnóstico
El diagnóstico de la DH debe realizarse en pacientes con lesiones clínicas compatibles y se basa en la combinación de criterios mayores y menores.
Los criterios principales incluyen historia de CD, presentación clínica típica e inmunofluorescencia directa (DIF) positiva.
La DIF es la herramienta diagnóstica fundamental y debe realizarse en piel sana, a 1–3 mm de la lesión activa, antes de iniciar dapsona o GFD, ya que ambos pueden inducir falsos negativos.
El hallazgo característico es el depósito granular de IgA en la unión dermoepidérmica y en las puntas papilares. Con menor frecuencia, pueden observarse depósitos en fibras elásticas, folículos pilosos, glándulas sudoríparas o vasos dérmicos. También puede detectarse fibrinógeno en los mismos sitios.
- Histología
Debe realizarse junto con DIF. Aunque no es específica, es sugestiva: infiltrado neutrofílico en papilas dérmicas con formación de microabscesos y, en lesiones ampollosas, clivaje subepidérmico. Puede observarse infiltrado mixto con neutrófilos, eosinófilos y linfocitos T.
- Serología
El ELISA para IgA anti-TG2 es útil tanto para el diagnóstico como para el seguimiento de la adherencia a la GFD. También puede emplearse ELISA para IgA anti-TG3, especialmente en subgrupos sin anticuerpos anti-TG2.
Los anticuerpos antigliadina no se recomiendan por falta de estandarización. La inmunofluorescencia indirecta para anticuerpos antiendomisio (EMA) presenta alta especificidad (cercana al 100%), con sensibilidad variable (60–90%).
La tipificación HLA-DQ2/DQ8 no se recomienda de rutina. La biopsia duodenal puede ser útil para evaluar el grado de enteropatía.
Figura Características histológicas e inmunopatológicas de la dermatitis herpetiforme. A) Detección de depósitos granulares de IgA a lo largo de la unión dermo-epidérmica por inmunofluorescencia directa. B, C) Desprendimiento subepidérmico con microabsceso neutrofílico (tinción de hematoxilina-eosina [HE], aumento original x 4). D) Detalle de un microabsceso neutrofílico (HE, x 20)
Trastornos asociados a la DH
Los pacientes con DH presentan menor mortalidad global y menor riesgo de eventos cerebrovasculares, posiblemente vinculado a estilos de vida más estrictos.
Se han descrito asociaciones con:
- Tiroiditis autoinmune (hasta 11%)
- Anemia perniciosa (1,3–3%)
- Diabetes tipo 1 (1–2%)
- Lupus eritematoso sistémico (baja frecuencia)
- Asociación anecdótica con dermatomiositis y síndrome de Sjögren
Un hallazgo relevante es la asociación con penfigoide bulloso (PB): la DH aumenta aproximadamente 22 veces el riesgo de PB, con una latencia media de 3 años. Este riesgo no se observa en CD aislada.
Asimismo, dado que todos los pacientes con DH presentan CD subclínica, existe mayor riesgo de linfoma no Hodgkin y neoplasias gastrointestinales, especialmente en los primeros 5 años.
Terapia
El pilar terapéutico es una GFD estricta y de por vida, evitando trigo, cebada y centeno. La avena solo es segura si no está contaminada. La mejoría clínica suele iniciarse en semanas o meses, con remisión completa promedio a los 2 años.
Es crucial confirmar el diagnóstico antes de iniciar la GFD.
La reintroducción de gluten provoca recaída cutánea en más del 80–90% de los pacientes y puede inducir nuevamente atrofia vellosa.
- Tratamiento farmacológico
Dado que las lesiones pueden persistir hasta 24 meses tras iniciar GFD, la mayoría requiere tratamiento sistémico.
. La dapsona es el tratamiento de primera línea, con respuesta rápida en pocas semanas. Dosis en adultos: inicio 25–50 mg/día, hasta 200 mg/día (máx. 2 mg/kg/día). Requiere control de G6PD previo y monitorización hematológica estricta.
. Alternativas: sulfonamidas (sulfasalazina, sulfapiridina), tetraciclinas con nicotinamida. Las guías europeas desaconsejan ciclosporina y corticoides sistémicos.

La reintroducción de gluten provoca recaída cutánea en más del 80–90% de los pacientes y puede inducir nuevamente atrofia vellosa
Otras dermatosis asociadas a enfermedad celíaca
Además de la DH, se han asociado a CD:
- Dermatitis atópica (DA), más frecuente en adultos y niños con CD
- Urticaria crónica (CU), con aumento de riesgo en estudios poblacionales
- Psoriasis, con mayor frecuencia de anticuerpos antigliadina y posible mejoría con GFD
- Alopecia areata (AA), con datos aún no concluyentes pero posibles beneficios con GFD
Estas asociaciones no tienen un mecanismo inmunológico claramente definido, aunque podrían compartir susceptibilidad genética e inmunorregulación común.
- Sensibilidad al gluten y trastornos neurológicos
La sensibilidad al gluten se ha asociado a ataxia cerebelosa (ataxia por gluten), neuropatía periférica y encefalopatía. Entre el 10% y el 22,5% de los pacientes con sensibilidad al gluten presentan manifestaciones neurológicas.
El diagnóstico puede apoyarse en la detección de anticuerpos anti-TG6. Los dermatólogos deben considerar derivación neurológica cuando corresponda.
- Sensibilidad al gluten no celíaca (NCGS) y piel
La sensibilidad al gluten no celíaca (Non-celiac gluten sensitivity, NCGS) se caracteriza por síntomas inducidos por gluten en ausencia de CD, con mejoría tras GFD. La prevalencia estimada oscila entre 0,5% y 13%, predominando en mujeres jóvenes.
La autoinmunidad no parece ser central; se postula un rol del sistema inmune innato y alteración de la barrera intestinal.
- Manifestaciones cutáneas en NCGS
Los datos son limitados, pero se han descrito:
. Lesiones eczematosas (≈45%)
. Lesiones urticariformes (≈36%)
. Lesiones psoriasiformes (≈9%)
. Prurito intenso, a veces síntoma aislado
En algunos casos se observaron lesiones similares a DH con depósito granular de C3 en la unión dermoepidérmica en DIF. La mejoría con GFD fue consistente.
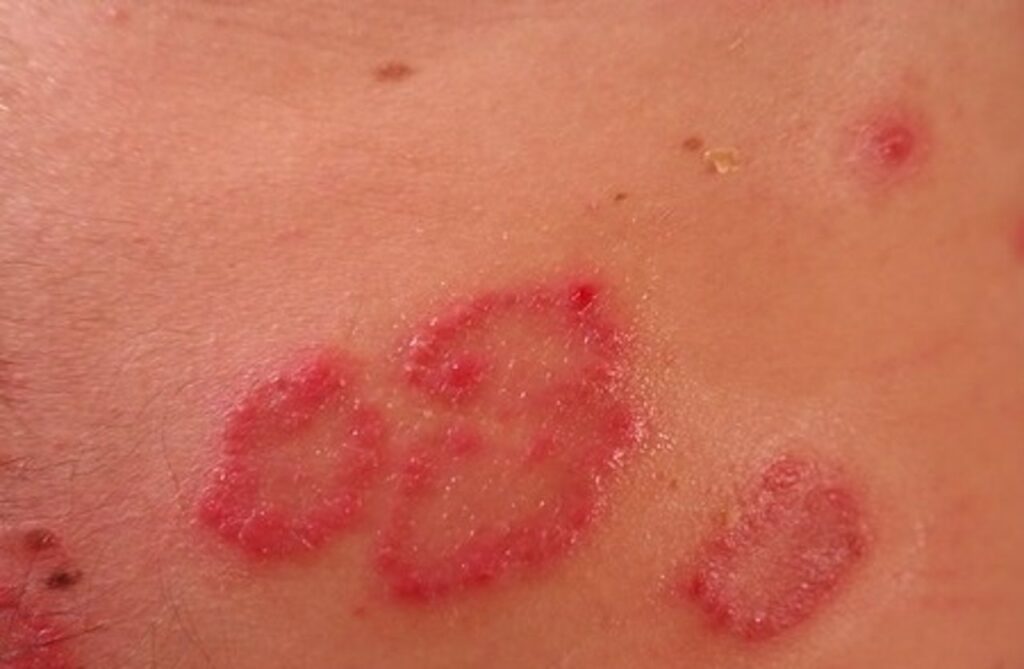
Además de la clásica asociación entre dermatitis herpetiforme y enfermedad celíaca, otras dermatosis pueden representar manifestaciones extraintestinales de los trastornos relacionados con el gluten
Conclusiones
Además de la clásica asociación entre DH y CD, otras dermatosis pueden representar manifestaciones extraintestinales de los trastornos relacionados con el gluten (GRDs).
Los dermatólogos deben considerar esta posibilidad, especialmente ante cuadros resistentes a corticoides, ya que algunos pacientes pueden experimentar mejoría significativa con GFD.
Estudios clínicos e inmunológicos en cohortes más amplias, particularmente en NCGS, podrían permitir definir un patrón cutáneo específico que facilite el diagnóstico temprano de enfermedad relacionada con el gluten.
Es clave realizar estudios clínicos e inmunológicos en cohortes más amplias para definir un patrón cutáneo específico que facilite el diagnóstico temprano de enfermedad relacionada con el gluten
Gluten y manifestaciones cutáneas
Fuente
Didona D, Maglie R, Solimani F. Gluten‐related skin disorders: clinical presentation, diagnostic and treatments. Dtsch Dermatol Ges. 2025 Jul 9;23(7):857–867.